Зависимость - перенапряжение
Cтраница 3
Уравнение, устанавливающее зависимость перенапряжения е от плотности тока (; аи b - постоянные. [31]
Уравнение (7.27) выражает зависимость перенапряжения диффузии от соотношения между поверхностной и объемной концентрацией молекул растворенного кислорода. Однако чтобы получить уравнение поляризационной кривой, это отношение должно быть представлено в виде функции плотности тока. [32]
В [193] подтверждена зависимость перенапряжения выделения водорода от расположения карбидообразую-щего металла в периодической системе. При переходе от MeIV C к MevC и MeVI C перенапряжение водорода в различных электролитах снижается на 0 2 - 0 3 в с достижением минимальных значений для карбидов хрома и вольфрама. [33]
Эти заключения несколько поясняют зависимость перенапряжения от кислотности среды, но количественной строгостью они не отличаются и полного согласия с опытом не дают. [34]
 |
Перенапряжение для выделения водорода и кислорода в 16 % - ном едком натре ( в вольтах. [35] |
В таблице 1 дана зависимость перенапряжения от материала электродов, плотности тока и температуры. [36]
На рис. 61 показана зависимость перенапряжения от плотности тока. Максимальное совершенство текстуры [ OJD1 ] никеля, электроосажденного из электролита, имеющего рН - 4 5 - 5 5, наблюдается при плотности тока 0 71 - 1 1 А / дм2, причем при изменении плотности тока до 0 2 А / дм2 в одну сторону и до 2 А дм2 в другую совершенство текстуры уменьшается медленно. [37]
 |
Типы электродов для электролиза воды. [38] |
В табл. 3 дана зависимость перенапряжения от расчетной плотности тока. При развитии поверхности электродов перенапряжение снижается. Для этого предложены особые конструкции электродов, у которых при одних и тех же габаритах рабочая поверхность больше, чем у гладких. [39]
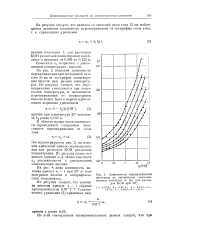 |
Зависимость перенапряжения кислорода на заряженном окисиони-келевом электроде от lg г для растворов КОН при 20. [40] |
На рис. 2 показана зависимость перенапряжения при постоянной силе тока 24 ма от логарифма концентрации щелочи при разных температурах. [41]
В § 73 разбирается зависимость перенапряжения реакции от времени по Коутецкому и Брдичке ш для р 1, причем стационарное распределение концентрации получается при предельном переходе t - оо. [42]
На рис. 21 представлена зависимость перенапряжения цинка от рН раствора, полученная в перхлоратных, сернокислых и хлористых растворах. [43]
Было высказано несколько причин зависимости перенапряжения от природы металла, в которых учитывались электронные структуры разряжающегося иона и выделяющегося металла, прочность связи ионов в растворе и в кристаллической решетке металла и др - Наиболее широкое распространение получило объяснение, основанное на различной склонности металлов к пассивации. [44]
Согласно Эрдей-Груц, характер зависимости перенапряжения от силы тока и механизм процесса при выделении серебра определяется природой электролита; например, первое условие соответствует растворам хлористого серебра в хлористом аммонии и цианистого серебра в цианистом калии; второе условие - растворам йодистого серебра в йодистом калии и окиси серебра в аммиачном растворе. В то же время при выделении серебра иа раствора хлористого или бромистого серебра в аммиаке перенапряжение оказывается линейной функцией lg /, из чего надо заключить, что в этом случае медленной стадией является разряд ионов. Однако трудно согласиться с этими выводами, так как кажется маловероятным, чтобы один и тот же металл мог выделяться тремя различными путями в зависимости от условий. [45]
Страницы: 1 2 3 4 5