Бисульфат - хинин
Cтраница 2
Ферстер рассчитал, что для флуоресцеина критическое расстояние переноса равно 50 А, а для хлорофилла - 80 А. Для бисульфата хинина, спектр поглощения которого значительно шире, значение емако ниже, а перекрывание меньше, получилось в 10 раз меньшее значение критического расстояния. Поэтому для самотушения флуоресценции путем переноса энергии требуются почти столь же высокие концентрации, как и для ударной дезактивации в маловязких растворителях при единичной эффективности встреч [ см. уравнение ( 86) ], но с дополнительным условием перекрывания спектров поглощения и испускания. Следовательно, можно быть уверенными, что если жидкий раствор разбавлен настолько, что в нем не происходит диффузионного самотушения флуоресценции, то в нем заведомо можно пренебречь и тушением по механизму дальнего переноса энергии. [16]
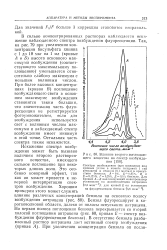
Это видно на рис. 48, где приведены спектры испускания разбавленного раствора бисульфата хинина, возбуждаемого светом ртутной лампы с длинами волн 405, 436 и 546 нм. Первая из этих длин волн слабо поглощается бисульфатом хинина и возбуждает широкую полосу флуоресценции. [17]
 |
Влияние второго поглощающего вещества на спектр возбуждения. [18] |
В сильно концентрированных растворах наблюдается искажение наблюдаемого спектра возбуждения флуоресценции. Так, на рис. 79 при увеличении концентрации бисульфата хинина с 1 до 10 мкг на 1 мл ( кривые А и Б) высота основного максимума возбуждения ( соответствующего максимальному поглощению) уменьшается относительно слабого максимума с меньшим волновым числом. [19]
Поляроид представляет собой пленку очень сильно дихроичного кристалла - герапатита ( периодат бисульфата хинина), полученного Герапатом в 1852 г. Чешуйка герапатита толщиной около 0 1 мм практически нацело поглощает один из лучей, являясь уже в таком тонком слое совершенным линейным поляризатором. [20]
Значения, приведенные в столбце 3, относятся к следующим стандартным растворам: Аа - антрацен в этаноле. А - антрацен в бензоле, ДФА - 9 10-ди-фенилантрацен в циклагексане, X - бисульфат хинина в разбавленной HjSO РБ - родамин Б в этаноле. [21]
 |
Исправление спектра возбуждения вручную. [22] |
Результаты, приведенные на рис. 94, иллюстрируют этот метод исправления. Верхняя кривая А характеризует относительную квантовую интенсивность возбуждающего света, сплошная кривая Б - спектр поглощения бисульфата хинина, а нижняя кривая В - регистрируемый ( неисправленный) спектр возбуждения. [23]
Однако для прибора с фильтрами суммарный фон флуоресценции в тысячу раз выше, чем чувствительность прибора, поэтому чувствительность метода определения бисульфата хинина лимитируется именно величиной и постоянством этого фона. Очевидно, что в данном случае невозможно использовать преимущества очень высокой чувствительности прибора, и утверждение, что чувствительность прибора с фильтрами эквивалентна концентрации бисульфата хинина 2 - 10 - 6 мкг / мл, может лишь ввести в заблуждение. Из табл. 45 следует, что в данных условиях нужно предпочесть прибор меньшей чувствительности, поскольку у него ниже суммарный фон, хотя этот последний все же выше предела чувствительности спектрофлуориметра. Разумеется, фон прибора с фильтрами можно снизить, например тщательным подбором фильтра и ( или) дополнительной очисткой веществ. Проблема фона люминесценции очень важна, и ниже мы неоднократно будем к ней возвращаться. [24]
Величину рассмотренных помех можно скорректировать, измеряя испускание чистого растворителя. То, что широкая полоса на кривой Б ( рис. 145) обусловлена именно рамановским рассеянием, можно подтвердить, возбуждая тот же спектр флуоресценции светом более короткой длины волны возбуждения: положение полосы флуоресценции бисульфата хинина не изменится, а дополнительная полоса сдвинется в коротковолновую сторону так, что ее расстояние ( в шкале волновых чисел) от линии возбуждающего света останется прежним. Помехи, усиливаются, если спектр флуоресценции имеет колебательную структуру. [25]
Это показывает, что в момент смешения активность ( -) - иона была меньше актквности () - иона, и поэтому при одинаковых концентрациях ( - Ь) - ион высаживается первым; в образце, простоявшем 1 день, активности выравнялись, при этом концентрация ( -) - иона возросла При последующем высаживании первым выделился рацемат [ так как активности () - и ( -) - ионов одинаковы ], а в конце выделились фракции с избытком ( -) - иона. Это является убедительным доказательством асимметрического превращения. Бисульфат хинина и ( н -) - / праис-этилендиаминкобальт ( III) также способны активировать этот ион. [26]
Мельюиш [162, 175], и оказалось, что квантовый выход равен 0 508 при концентраций 5 - Ю 3 М с константой самотушения 14 5, соответствующей квантовому выходу при бесконечном разбавлении, равному 0 546 при 25 С или 0 553 при 20 С. Стандартный бисульфат хинина ( молекулярный вес 548 6) лучше всего готовить многократной перекристаллизацией соли из воды. Он кристаллизуется с семью молекулами воды, которую удаляют, высушивая образец в вакууме над силикагелем. [27]
Чувствительность прибора соответствует той концентрации бисульфата хинина, которая нужна для того, чтобы сигнал был равен шуму, отвечающему флуктуациям темпового тока. [28]
Показатель абсолютной чувствительности флуоресценции используется также для предсказания возможной чувствительности определенного прибора. В этом случае необходимо принять во внимание характеристики прибора. Предположим, например, что чувствительность спектрофлуориметра для обнаружения бисульфата хинина с возбуждением светом 366 нм известна и нужно определить чувствительность в случае тионина. Показатель абсолютной чувствительности тионина ( табл. 47, столбец 8) составляет 0 038 ( 0 00028 / 0 0073) от показателя бисульфата хинина. Последний показывает, что чувствительность в максимуме флуоресценции тионина составляет приблизительно 0 6 от чувствительности в максимуме флуоресценции бисульфата хинина. [29]
 |
Промывной цилиндр для хинина. [30] |
Страницы: 1 2 3