Определение - двухвалентное железо
Cтраница 1
Определение двухвалентного железа возможно только в водах, не содержащих относительно большого количества органических веществ, связывающих железо в комплексные соединения, поскольку в процессе разложения этих комплексов железо окисляется. [1]
Определение двухвалентного железа основано на прямом титровании Fe - ионов стандартным раствором перманганата калия в кислой среде. [2]
Определение двухвалентного железа в солянокислом растворе имеет большое практическое значение при определении его в сплавах, металлах, рудах, которые обычно растворяют в соляной кислоте. [3]
Определение двухвалентного железа в сульфате железа или в соли Мора ведут методом прямого титрования. Навеску тонкорастертой соли железа растворяют в 10 % - ной серной кислоте, разбавляют в мерной колбе водой и аликвотную часть раствора пипеткой переносят в колбу для титрования. Следует объяснить учащимся, что большой избыток серной кислоты необходим для уменьшения гидролиза сульфата двухвалентного железа. В отличие от щавелевой кислоты соли двухвалентного железа титруют при комнатной температуре, чтобы избежать окисления ионов железа кислородом воздуха. [4]
Применяется для количеств, определения двухвалентного железа, а также мн. [5]
Плавиковую кислоту, применяемую при определении двухвалентного железа титрованием перманганатом или бихроматом, очищают от примесей органических веществ. Для этого к плавиковой кислоте в платиновой чашке добавляют растертый в порошок пер-манганат калия до получения интенсивного фиолетового окрашивания, сохраняющегося длительное время. [6]
Раствор кремнемолибденовой кислоты применяют как индикатор при определении двухвалентного железа титрованием раствором бихромата. [7]
Наиболее важное применение фосфорная кислота находит при определении двухвалентного железа в хромитах [4.298, 4.314- 4.316], ферритах [4.317-4.322] и различных силикатах [4.323, 4.324], которые не растворяются во фтороводородной кислоте. Воздух удаляют из образца и кислоты, поэтому железо ( II) не окисляется при разложении и его можно определить в растворе. Другой вариант метода определения железа ( II) заключается в обработке пробы кислотой, в которую введено известное количество окислителя, и в определении окислителя обратным титрованием после полного растворения пробы. Следует иметь в виду, что если разложение пробы проводят в атмосфере диоксида углерода, то СО2 восстанавливается до СО, а затем окисляется в растворе, что может привести к значительным погрешностям при использовании для анализа окислительно-восстановительных методов. Для определения FeO в турмалине пробу обрабатывают Н3РО4, содержащей NH4F и KHF2 при 210 - 220 С. [8]
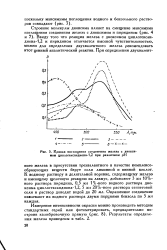 |
Кривая поглощения соединения железа с диоксимом циклогександиона-1 2 при различном рН. [9] |
Ввиду того что реакция железа с диоксимом циклогексан-диона-1 2 и пиридином отличается высокой чувствительностью, можно для определения двухвалентного железа рекомендовать этот ценный аналитический реактив. [10]
Примером внешнего индикатора служит феррицианид калия Кз [ Fe ( CN) e ], употребляемый при определении двухвалентного железа хроматометри-ческим методом. [11]
Раствор переводят в коническую колбу емк. После определения двухвалентного железа в колбу вносят металлический кадмий и восстанавливают железо и титан при умеренном нагревании в течение 10 - 15 мин. В присутствии фтороборной кислоты раствор не окрашивается в фиолетовый цвет, характерный для ионов Ti3, тем не менее HBF4 не препятствует восстановлению титана до трехвалентного и последующему титрованию его раствором перманганата калия с индикатором вольфраматом натрия. [12]
С появлением сосудов из церезина и полиэтилена отпала необходимость в повторных перегонках плавиковой кислоты, за исключением, может быть, некоторых особых случаев. Обычными примесями в плавиковой кислоте являются железо, соляная кислота и органические вещества. Влияние первых двух может быть учтено тщательно проведенными контрольными опытами, а примесь органических веществ вообще влияния не оказывает, за исключением двух случаев анализа: определения двухвалентного железа в горных породах и определения пятивалентного мышьяка в стеклах. [13]
Определение содержания металлического железа основано на взаимодействии его с ионами металла, имеющего более высокий электродный потенциал. С этой целью навеску губчатого железа обрабатывают [170] нейтральным раствором сернокислой меди. Металличеркое железо при этом переходит в раствор в двухвалентной форме, а медь выделяется в элементарном состоянии эквивалентно перешедшему в раствор железу. Количество металлического железа устанавливают путем определения двухвалентного железа в растворе перманганатным методом. Окислы железа при этой обработке остаются без изменения. [14]
Страницы: 1