Зависимость - потенциал
Cтраница 3
Зависимость потенциала анода от плотности тока при электрополировании меди в растворах фосфорной кислоты иллюстрируется кривыми рис. 33 ( см. стр. [31]
Зависимость потенциала полуоквсления редокс-системн метиленоввй синий - лейкометиленовнй синий от рН внешнего раствора. [32]
Нернстов-ская зависимость потенциала от активности ионов РЬ2 выполняется во всем интервале его функционирования. [33]
Зависимость 1-электродного потенциала f медного диска и 2 - скорости коррозии ( К) от поляризующего действия катионов фона П при 2600 об / мин, когда растворы содержат 0 4 г-ион / л Си ( И) и 3 г-ион / л хлора. [34]
 |
Изменение Рпо зависимости от а в растворах хлоридов. [35] |
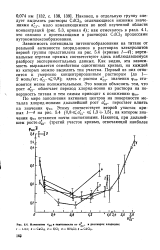
Зависимость потенциала питтингообразования на титане от реальной активности хлорид-ионов в растворах электролитов первой группы представлена на рис. 5.4 ( кривые / - 4); вертикальные отрезки прямых соответствуют здесь наблюдавшемуся разбросу экспериментальных данных. Как видно, эта зависимость выражается семейством однотипных кривых, на каждой из которых можно выделить три участка. Первый из них относится к умеренно концентрированным растворам ( до 1 - 2 моль / кг; асг 0 8); здесь с ростом а сг значения pno становятся менее положительными. Это можно объяснить тем, что рост UCP облегчает переход хлорид-ионов из раствора на поверхность титана и тем самым приводит к понижению фпо. [36]
Зависимость потенциала пробоя ( кривая А) и механической прочности связи ( кривая Б) от концентрации KF ( I) и NaF ( II) при выделении осадков цинка и никеля на алюминии при 25 С. [37]
Зависимость потенциала пробоя ( кривая А) и механической прочности связи ( кривая Б) от плотности тока при выделении осадков цинка и никеля на алюминиевую подложку при 25 С. [38]
Зависимость потенциала точки эквивалентности от аналитической концентрации очень слаба, а от рН очень сильна. Изменение рН на единицу меняет потенциал в точке эквивалентности на 0 12 в. Конечно, изменение кислотности и аналитической концентрации бихромата подействует на формальный потенциал пары хром-бихромат, так как доли Cr ( VI) и Cr ( III), связанные в других соединениях ( например, НСгО7, СгО -, СгОН2), изменятся. [39]
Зависимость потенциала кислородного электрода от рН имеет вид прямой с наклоном - 0 0591 в на единицу рН, как в случае водородного электрода. Как показывает (4.21), увеличение Ю на единицу ( что означает уменьшение парциального давления кислорода на целый порядок) сопровождается уменьшением потенциала кислородного электрода на величину, близкую к 15 мв. [40]
Зависимость потенциала амальгамного электрода от силы внешнего тока выражается уравнением Я. [41]
Зависимость потенциала окислительно-восстановительного электрода от рН не означает, что его можно уподобить газообразному водородному электроду. [42]
Зависимость потенциала хлорсеребряного электрода от активности ионов хлора может быть выведена следующим образом. [43]
Зависимость потенциала окислительно-восстановительного электрода от рН не означает, что его можно уподобить газообразному водородному электроду. [44]
Зависимость потенциала кислородного электрода от рН имеет вид прямой с наклоном - 0 0591 в на единицу рН, как в случае водородного электрода. [45]
Страницы: 1 2 3 4