Зависимость - потенциал - стеклянный электрод
Cтраница 1
Зависимость потенциала стеклянного электрода от концентрации ионов нелинейна. [1]
Вывод уравнения зависимости потенциала стеклянного электрода от рН основан на предположении равенства при равновесии электрохимических потенциалов водородных ионов в стекле и электрохимических потенциалов ионов водорода в растворе. Такое предположение может быть сделано по отношению к любому электрохимическому равновесию на границе любых двух фаз, независимо от механизма действия электрода. [2]
Вывод уравнения зависимости потенциала стеклянного электрода от рН основан на том предположении, что при равновесии электрохимический потенциал водородных ионов в стекле равен электрохимическому потенциалу ионов водорода в растворе - Следует иметь в виду, что такое предположение может быть сделано по отношению к любому электрохимическому равновесию на границе любых двух фаз, независимо от механизма действия электрода. [3]
Вывод уравнения зависимости потенциала стеклянного электрода от рН основан на предположении равенства при равновесии электрохимических потенциалов водородных ионов в стекле и электрохимических потенциалов ионов водорода в растворе. Такое предположение может быть сделано по отношению к любому электрохимическому равновесию на границе любых двух фаз, независимо от механизма действия электрода. [4]
На графике изображена зависимость потенциала стеклянного электрода относительно каломельного электрода сравнения от объема прибавленного титранта для смесей четырех сильных кислот. Кривая А свидетельствует о четком разделении хлорной и серной кислоты, а также о двухосновном характере серной кислоты. Несмотря на то, что первая точка эквивалентности относится к сумме серной и хлористоводородной кислоты, объем титранта, добавленного между первой и второй точками эквивалентности, соответствует только серной кислоте, поэтому количество хлористоводородной кислоты в пробе можно вычислить по разности. Кривая Г показывает, что смесь азотной и хлористоводородной кислот в метилизобутилкетоне разделить нельзя. [5]
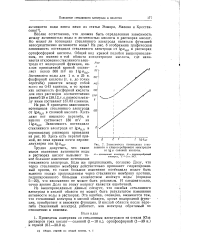 |
Зависимость потенциала стеклянного и хлоросеребряного электродов от lg а соляной кислоты. [6] |
На рис. 9 приведена зависимость потенциала стеклянного электрода от lgeHO в соляной кислоте. [7]
В этих работах подробно изучена зависимость потенциала стеклянного электрода от концентрации ионов щелочных и некоторых других металлов. Было замечено, что десятикратное изменение концентрации ионов щелочных металлов при определенных условиях может изменять потенциал стеклянного электрода по отношению к каломельному электроду на 50 - 55 мв. Как видно, расхождение между опытными и теоретическими данными не очень большое. [8]
Таким образом, если не количественно, то качественно, а возможно и полуколичественно, уравнения обобщенной теории передают зависимость потенциала стеклянного электрода от активностей ионов в растворе в соответствии с физическим смыслом теории и физическим смыслом характерных констант в ее уравнениях. [9]
В случае, если измерение со стеклянным электродом производится на потенциометре, имеющем шкалу в милливольтах, калибрирование производится путем получения графика зависимости потенциала стеклянного электрода от рН буферных растворов. [10]
Дальнейшие исследования стеклянного электрода, проведенные автором вместе с Францевич-Заблудовской и Александровой, показали, что и в других растворителях ( спирты, кетоны, кислоты) характер зависимости потенциала стеклянного электрода от рН для водных и неводных растворов один и тот же, с тем отличием, что обычно отклонения в неводных растворах наступают несколько раньше как в кислых, так и в щелочных растворах. [11]
 |
Зависимость потенциала стеклянного электрода от рН раствора. [12] |
& й - рН в кислой и щелочной областях одинаковы по величине и обратны по знаку. Зависимость потенциала стеклянного электрода от рН выражается кривой с максимумом ( рис. 7.1), положение которого зависит от сорта стекла, и определяется его константой обмена. [13]
Основной недостаток стеклянного электрода состоит в том, что он дает линейную зависимость между потенциалом и рН не при всех его значениях, а только в некоторой области рН, причем для разных электродных стекол область линейной зависимости различна. Обычно характер зависимости потенциала стеклянного электрода от рН таков: в некоторой области между потенциалом и рН имеет место линейная зависимость с наклоном 0 059 вольт на единицу ipH; затем в кислых и щелочных растворах наступают отклонения. Полная кривая зависимости потенциала от рН имеет симметричный вид: в щелочной области наблюдается прямолинейная зависимость потенциала от рН с тем же углом наклона, что и в средней области рН5 но противоположная по направлению. Значения рН, при которых наблюдаются перегибы, различны для различных стекол. Эти ограничения сильно зависят от состава стекла. Близкое по составу стекло Мак-Иннеса и Дола - - Кернинг 015 ( см. ниже) дает отклонения в более кислых растворах и более поздние отклонения в щелочной области. [14]
Для калибрирования стеклянного электрода необходимо иметь 2 - 3 буферных раствора, рН которых точно установлен при помощи водородного электрода. Затем измеряют потенциал стеклянного электрода в этих растворах и строят график зависимости потенциалов стеклянного электрода от рН раствора. [15]
Страницы: 1 2