Зависимость - потенциал - индикаторный электрод
Cтраница 1
Зависимость потенциала индикаторного электрода Е, измеренного относительно электрода сравнения, от объема прибавленного титранта представляет собой интегральную кривую титрования. [1]
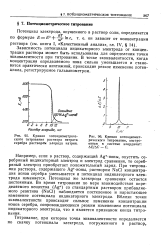 |
Кривая потенциометриче-ского титрования раствора нитрата серебра растворам хлорида натрия.| Кривая потенциомет-рического титрования, построенная в системе координат. Л. / ДС - С. [2] |
Зависимость потенциала индикаторного электрода от концентрации раствора может быть использована для определения точки эквивалентности при титровании. В точке эквивалентности, когда концентрация определяемого иона сильно уменьшается и становится практически ничтожной, происходит резкое изменение потенциала, регистрируемое гальванометром. [3]
Рассмотрим теперь зависимость потенциала индикаторного электрода от потенциала основного электрода при его анодной и катодной поляризации. [4]
При рассмотрении зависимости потенциала индикаторного электрода от концентрации НВЧ в объеме раствора необходимо иметь ввиду два обстоятельства. Во-первых, потенциал электрода определяется концентрацией НВЧ на поверхности электрода. [5]
Таким образом, зависимость потенциала индикаторного электрода от объемной концентрации одновалентных ионов отличается от зависимости потенциала этого электрода от поверхностной концентрации одновалентных ионов наличием, в случае недостаточно интенсивного перемешивания, участка независимости фи от [ М 10 вблизи равновесного потенциала. [6]
 |
Схема индикационной цепи при амперометрическом определении конечной точки титрования с двумя поляризованными электродами. [7] |
Изобразить графически кривую кулонометрического титрования в виде зависимости потенциала индикаторного электрода ( мВ) от времени электролиза ( с), а также дифференциальную кривую A. [8]
 |
Схема индикационной цепи при амперометрическом определении конечной точки титрования с двумя поляризованными электродами. [9] |
Изобразить графически кривую кулонометрического титрования в виде зависимости потенциала индикаторного электрода ( мВ) от времени электролиза ( с), а также дифференциальную кривую AE / At - t, по которой находят конечную точку титрования. [10]
Как видно из ( 41) и ( 42), зависимость потенциала индикаторного электрода от объемной концентрации одновалентных ионов нельзя выразить в явном виде. [11]
Потенциометрическое титрование объединяет способы определения конечной точки титрования ( КТТ), основанные на зависимости потенциала индикаторного электрода от объема добавленного титранта. Примеры кривых такой зависимости представлены на рис. 7.1. По сравнению с прямыми измерениями полученные при потенциометрическом титровании данные более точно и правильно характеризуют концентрацию определяемого вещества, поскольку не зависят от его активности. Кроме того, в методах потенциометрического титрования к электродам предъявляются менее жесткие требования в отношении стабильности потенциала и крутизны наклона электродной функции. Электроды, непригодные для прямых потенциометрических измерений, могут отвечать требованиям потенциометрического титрования. Наконец, методы потенциометрического титрования позволяют находить концентрацию анализируемого компонента даже в присутствии мешающих ионов, если титрант селективно взаимодействует с определяемым веществом. [12]
Для этой цели часто используют платиновый электрод в сочетании с насыщенным или нормальным каломельным электродом. Удобно вести измерения потенциала индикаторного электрода с помощью ламповых потенциометров ЛП-5, ЛП-58 или ЛПУ-01. На основе полученных данных строят график зависимости потенциала индикаторного электрода от количества добавленного титранта и на кривой находят конечную точку. [13]
 |
Гальванический элемент с электролитическим мостиком ( а и потенциалы в таком элементе ( б. [14] |
Если некомпенсированный диффузионный потенциал в течение проведения опыта остается постоянным, его можно объединить с другими постоянными величинами. Таковыми являются потенциал электрода сравнения и стандартный потенциал индикаторного электрода. Обозначим объединенную постоянную величину Ег.э. ЭДС гальванического элемента тогда алгебраически складывается из этой величины и члена, показывающего зависимость потенциала индикаторного электрода от активностей ионов, участвующих в электродной реакции. [15]
Страницы: 1 2