Зависимость - адсорбционный потенциал
Cтраница 1
Зависимость адсорбционного потенциала от количества адсорбированного пара называется характеристической кривой. Зная уравнение характеристической кривой Е i ( w), часто можно трудоемкую экспериментальную работу заменить несложными расчетами. [1]
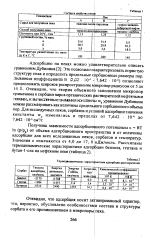 |
Термодинамические характеристики адсорбции растворителей. [2] |
Получены зависимости адсорбционного потенциала е RT In ( p / ps) от объема адсорбционного пространства и от величины адсорбции для всех иследоваиных пеков, сорбатов и температур. Значения е изменяются от 4 0 до 17, 0 кДж / моль. [3]
Можно построить график зависимости адсорбционного потенциала от веса адсорбированного газа и получить характеристические кривые сродства, которые показывают, что для любого данного адсорбента адсорбционный потенциал зависит только от корня квадратного из величины когезии газа. Здесь Wx - вес адсорбированного пара, а А - плотность пара, адсорбированного в виде жидкости при температуре эксперимента. [4]
Характеристической кривой называется кривая зависимости адсорбционного потенциала от объемов адсорбционных пространств между поверхностью адсорбента и эквипотенциальными поверхностями. [5]
Для данного адсорбента при любой температуре зависимость адсорбционного потенциала от объема адсорбционного пространства выражается одним и тем же уравнением или одной кривой. [6]
Жидкое состояние адсорбата в порах позволяет заменить зависимость адсорбционного потенциала от расстояния между поверхностью адсорбента и соответствующим слоем адсорбата ( которое для пористого адсорбента определить не представляется возможным) на функцию от объема жидкого адсорбата. [7]
Как видно из рис. XIX, 46, зависимость адсорбционного потенциала от объема адсорбционного пространства для данного адсорбита практически не зависит от температуры и выражается одной кривой t - j ( w), называемой характеристической кривой. [8]
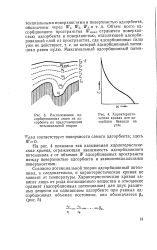 |
Расположение адсорбированных слоев на адсорбенте по представлениям потенциальной теории.| Характеристическая кривая для адсорбции бензола на угле. [9] |
На рис. 4 показана так называемая характеристическая кривая, отражающая зависимость адсорбционного потенциала е от объемов W адсорбционных пространств между поверхностью адсорбента и эквипотенциальными поверхностями. [10]
Гиббса; температуры стеклования и плавления ( размягчения) пеков и температуры жидко-кристаллических переходов в них; зависимости адсорбционного потенциала от величины объема адсорбционного пространства. [11]
 |
Потенциальная характеристическая кривая адсорбции. С. [12] |
В теории Поляни сделано допущение, что практически все адсорбированное вещество находится на поверхности в жидком состоянии. Это позволяет заменить зависимость адсорбционного потенциала от расстояния ( которое для пористого адсорбента определить не представляется возможным) на функцию от объема жидкого адсорбата. [13]
Для характеристики адсорбента необходимо знать распределение адсорбционного объема между различными значениями адсорбционного потенциала. Характеристические кривые передают зависимость адсорбционного потенциала от объема V, занимаемого адсорбционной жидкостью. [14]
Разумеется, что ошибка, допускаемая при этом, будет тем больше, чем сложнее группа атомов, которая объединяется единым силовым центром. Если усреднить эти расхождения и принять, что энергия взаимодействия квадруполей составляет примерно 10 % энергии взаимодействия диполей, то на графике в координатах Е ( п) ( где п - число одинаковых звеньев, например, групп СН2) для достаточно длинной молекулы углеводорода можно получить прямую, отражающую зависимость адсорбционного потенциала от числа групп СН2 в нормальной углеводородной цепи. [15]
Страницы: 1