Определение - количество - электричество
Cтраница 2
Метод состоит в определении количества электричества, необходимого для восстановления окисла либо до металла, либо до низшего окисла. Впервые он был использован Эвансом и Банвистером [614] для определения толщины пленки йодистого серебра, образующейся нз металлическом серебре, по количеству электричества, требующегося для восстановления пленки до металла. [16]
Кулонометрия состоит в определении количества электричества, расходуемого в ходе электрохимической реакции. [17]
Электролизеры, служащие для определения количества электричества, называются кулометрами. [18]
Электролизеры, служащие для определения количества электричества, называются кулометрами. Для точной работы куло-метра необходимо, чтобы в нем протекал лишь один электрохимический процесс без каких-либо побочных реакций и чтобы продукты электролиза поддавались точному взвешиванию или измерению. Простейшим и наиболее доступным из них является медный кулометр. [19]
Во всех случаях достоверность определения количества электричества зависит от точности установления титра и измерения израсходованного объема стандартного раствора. Обращение с титрационными куло-нометрами несложно; но они пригодны для определения лишь сравнительно больших количеств электричества. [20]
Весовые кулонометры основаны на определении количества электричества, прошедшего через систему по привесу металла катода. В простейшем виде он состоит из платинового тигля 4, служащего катодом, и серебряного анода 2, который подвешивается на стеклянный крючок. Между электродами на стеклянном кольце / находится пористый сосуд 3 - диафрагма, препятствующая возникновению побочных реакций. [21]
Кулопометрический метод основан на определении количества электричества, расходуемого на электрохимическую реакцию. Вариант кулонометрического титрования можно сравнить с визуальным титрованием: концентрации раствора соответствует величина тока, а объему титранта - время его пропускания. Для обнаружения ТЭ применяют как индикаторные, так и электрохимические методы. [22]
Кулонометрические методы основаны на определении количества электричества, которое расходуется в электрохимической реакции. [23]
Весовые кулонометры основаны на определении количества электричества, прошедшего через систему по привесу металла катода. В простейшем виде он состоит из платинового тигля 4, служащего катодом, и серебряного анода 2, который подвешивается на. Между электродами на стеклянном кольце / находится пористый сосуд 3 - диафрагма, препятствующая возникновению побочных реакций. [24]
Кулонометрический анализ заключается в определении количества электричества, расходуемого в ходе электрохимической реакции. [25]
Если воспользоваться медным кулонометром для определения количества электричества, то т будет равно отношению количеств меди, выделившейся при разрядке и зарядке. [26]
Если воспользоваться медным кулонометром для определения количества электричества, то j будет равно отношению количеств меди, выделившейся при разрядке и зарядке. [27]
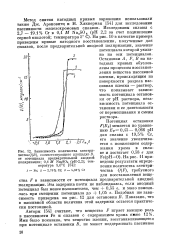 |
Зависимость количества электричества. (. 8, соответствующего площадке В, от потенциала предварительной анодной поляризации. 0 1 М Na2S04 ( рН - 2 2. температура 5 0 С. [28] |
На рис. 11 приведены результаты определения количества электричества Q ( F), требуемого для восстановления вещества F в зависимости от потенциала предварительной анодной поляризации. Эта задержка почти не наблюдалась, если анодный потенциал был менее положителен, чем 0 55 в, и мало изменялась при смещении потенциала до 1 05 в. Подобная же зависимость приведена на рис. 12 для остановки В. Показано, что в пассивной области величина этой задержки остается практически постоянной. [29]
 |
Электрохимический датчик давления.| Электрохимический интегратор. [30] |
Страницы: 1 2 3 4