Зависимость - термодинамический потенциал
Cтраница 1
Зависимость термодинамических потенциалов от их естественных переменных описывается основным уравнением термодинамики, которое объединяет первое и второе начала. [1]
Зависимость термодинамического потенциала от температуры выражается равенством AZ 34 7 Т-2530, откуда следует, что конверсия пропилена и воды в изопропиловый спирт с повышением температуры уменьшается. [2]
 |
Зависимость термодинамического потенциала от температуры.| Различные формы камерного электрода. [3] |
На рис. 78 показана зависимость термодинамического потенциала реакций от температуры. Первая реакция возможна начиная с / 1240 С ( отрицательный знак свободной энергии), вторая невозможна при доступной температуре. Хотя метод оценки направления химической реакции по изменению изобарно-изотермического потенциала приближенный, он до некоторой степени позволяет управлять химическими процессами в электроде и использовать их для повышения чувствительности и точности определений. Химические реакции в электроде широко применяют в аналитической практике. [4]
 |
Равновесное состояние. [5] |
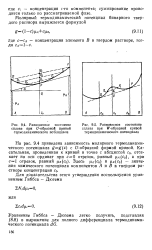
На рис. 9.4 приведена зависимость молярного термодинамического потенциала gg ( c) с / - образной формой кривой. [6]
 |
Схематическая зависимость термодинамических потенциалов идеального газа от его объема. [7] |
На рис. 38 схематически изображены зависимости термодинамических потенциалов идеального газа от его объема. [8]
 |
Зависимость термо. [9] |
На рис. IV, 2 схематически изображены зависимости термодинамических потенциалов идеального газа от его объема. [10]
Опыт тем не менее подтверждает аналитический вид зависимости термодинамического потенциала от магнитной поляризации в области температур, не слишком близких к точке Кюри. [11]
Для определения фазового состава оказывается достаточным знать зависимости термодинамических потенциалов фаз от их состава. [12]
Следуя изложенному выше методу, можно получить явный вид зависимости термодинамического потенциала Ф от аргументов Т и Р, а также от внешних параметров а - ( если таковые имеются), входящих в гамильтониан. Явное выражение для потенциала Ф и уравнение (1.5.35) позволяют найти любые характеристики равновесного изотермо-изобарического ансамбля. [13]
Для дальнейшего, как и в случае одно-компонентных фаз, интересна зависимость термодинамического потенциала от давления при постоянных температуре и составе. [14]
Термодинамическая теория фазового равновесия приводит к количественному объяснению диаграмм состояния, если известна зависимость термодинамических потенциалов фаз от соответствующих переменных. Однако вопрос об указанной зависимости выходит за рамки феноменологической термодинамики и в термодинамике гетерогенных систем одной из важных задач оказывается исследование тех закономерностей диаграмм состояния, которые можно установить без использования конкретного вида характеристических функций. [15]
Страницы: 1 2