Определение - константа - кислотная диссоциация
Cтраница 1
Определение констант кислотной диссоциации на основании изучения гидролиза в растворах чистой соли металла возможно только для самых сильных акво-кислот. В случае очень слабых акво-кислот слишком большую роль играют небольшие примеси кислот или оснований в исследуемой соли. По этой причине многочисленные исследования гидролиза солей металлов, описанные в литературе, практически не имеют значения. [1]
Для определения констант кислотной диссоциации комплексных соединений широко используются потенциометрический и спектрофотометрический методы. Имеются работы по применению для этой цели ИК спектроскопии и метода ПМР. Однако два последних следует считать корреляционными, так как их использование основано на взаимосвязи определенного рвойства комплексного соединения с его способностью к кислотной Диссоциации. [2]
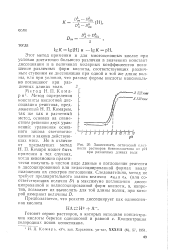 |
Зависимость оптической плотности растворов бензоилацетона от рН при различных длинах волн. [3] |
Метод определения L константы кислотной диссоциации реактива, предложенный Н. П. Комарем, так же как и расчетный метод, основан на совместном решении двух уравнений: уравнения основного закона светопогло-щения и закона действующих масс. Но в отличие от предыдущих метод Н. П. Комаря может быть применен в тех случаях, когда невозможно практически получить в чистом виде данные о поглощении реагента в диссоциированной или недиссоциированной формах ввиду наложения их спектров поглощения. [4]
При определении констант кислотной диссоциации иона этилендиаммония водно-спиртовые растворы, содержащие 0 2 М НС1О4 и 0 05 М Ва ( 0164) 2, титровались 9.54 М раствором этилендиамина. [5]
Распространенным методом определения констант кислотной диссоциации является также спектрофотометрический. Для применения этого метода Необходимо, чтобы существовала область спектра, в которой молярные коэффициенты погашения кислотной и основной форм заметно различались. [6]
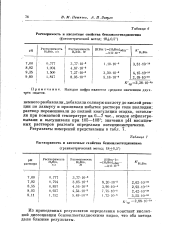 |
Растворимость и кислотные СЕОЙСТВЗ бегооилметилдиоксвма. [7] |
Из приведенных результатов определения констант кислотной диссоциации бензоилметилдиоксима видно, что оба метода дали близкие результаты. [8]
Даны также спектрофотометрические методы определения констант кислотной диссоциации органических реагентов, проявляющих слабую кислотную функцию. Все эти примеры ярко показывают преимущество спектрофотометров - приборов, имеющих высокую степень монохроматизации. [9]
В статье приведены характеристики кислотно-основных свойств комплексных соединений, являющихся кислотами Врснстеда, и методы определения констант кислотной диссоциации этих комплексов. [10]
К растворам соляной кислоты, содержащим хлорид калия ( см. табл. 51 и 52), добавляли хлорид бария, как уже отмечалось, в целях определения констант кислотной диссоциации этилендиамина точно при тех же концентрациях соли, как и в растворах, в которые вводили ионы металла-комплексообразо-вателя. Поправка, внесенная в этом случае, хотя и небольшая, но все же имеет некоторое значение. [11]
К растворам соляной кислоты, содержащим хлорид калия ( см. табл. 51 и 52), добавляли хлорид бария, как уже отмечалось, в целях определения констант кислотной диссоциации этилендиамина точно при тех же концентрациях соли, как и в растворах, в которые вводили ионы металла-комплексообразо-вателя. Поправка, внесенная в этом случае, хотя и небольшая, но все же имеет некоторое значение. [12]
В работе I5J показана также возможность применения ФМБП для выделения некоторых радиоизотопов без носителя. В настоящем сообщении приведены результаты определения константы кислотной диссоциации реагента и его константы распределения в системе изоамиловый спирт - вода. [13]
Страницы: 1