Определение - константа - устойчивость
Cтраница 2
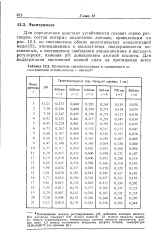 |
Изменение светопоглощения в зависимости от соотношения этилендиамин - оксалата. [16] |
Для определения констант устойчивости готовят серию растворов, состав которых аналогичен данным, приведенным на рис. 12.1, но соотношение общих аналитических концентраций меди ( II), этилендиамина и оксалат-иона поддерживается постоянным, а соотношение свободного этилендиамина и оксалата регулируют, изменяя рН добавлением азотной кислоты. [17]
Для определения констант устойчивости комплексных соединений также существует ряд фотометрических методов. [18]
Для определения констант устойчивости комплексных соединений часто используют зависимость среднего молярного коэффициента погашения е системы от концентрации лиганда. [19]
Основы определения констант устойчивости по данным о растворимости разрабатывались в течение многих лет [83-87], так что теперь существует реальная возможность определять последовательные константы устойчивости комплексов на основании измерения растворимости. [20]
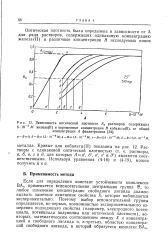
При определении констант устойчивости комплексов было обнаружено, что вымывание р.з.э. происходит только при доведении рабочего раствора комплексона 2 - ОПДТУ при концентрациях 1.10 - 3 - 3.10 - 3 М до рН 6 - 7 5 ( рН создавали прибавлением аммиака), причем при вымывании р.з.э. со смолы наблюдается резкое возрастание кислотности фильтратов. Так, в опытах с тербием, при 1 % - ной его загрузке и концентрации комплексона 1.10 3 М, в процессе вымывания кислотность среды возрастает от исходного значения рН 8 15 до рН 4 4 ( рис. 1); при этом минимум на кривой изменения рН соответствует максимуму на кривой вымывания. Аналогичные результаты были получены и для других р.з.э. Следует отметить, что при переходе ст лантана к лютецию кислотность фильтрата усиливается. [21]
При определении констант устойчивости ионитных комплексов следует особое внимание уделить подбору лиганда L: и лиганд, и образующийся растворимый комплекс не должны сорбироваться ионитом. Поэтому при определении констант устойчивости комплексов, образующихся в фазе катионитов и амфолитов, лиганд и растворенный комплекс должны быть анионами, а при определении констант устойчивости анионитных комплексов низкомолекулярный лиганд должен быть нейтральной молекулой, а образующийся растворенный комплекс - катионом. [22]
Ледена для определения констант устойчивости последовательной экстраполяцией ( см. гл. [23]
 |
Зависимость оптической плотности As растворов, содержащих. [24] |
Если для определения констант устойчивости комплексов ВА применяется вспомогательная центральная группа 93, то любое изменение концентрации свободного лиганда должно вызвать заметное изменение свойства X, которое наблюдается экспериментально. [25]
Преимущества метода определения констант устойчивости с ртутным электродом заключаются в быстром установлении равновесия. [26]
Преимущества метода определения констант устойчивости с ртутным электродом очевидны. [27]
Преимущества метода определения констант устойчивости с ртутным электродом заключаются в быстром установлении равновесия. [28]
Другой метод определения констант устойчивости заключается в вычислении из экспериментальных данных некоторой величины, зависимость которой от концентрации лиганда является алгебраической функцией - линейной или степенной. Такой подход является одним из вариантов метода Ледена. [29]
Кинетический метод определения констант устойчивости имеет ряд существенных недостатков даже по сравнению со спектрофотометрией, с которой он, в принципе, несколько сходен. Начальную скорость реакции М нельзя измерить непосредственно, ее надо определить экстраполяцией на нулевое время, что увеличивает некоторую неопределенность в экспериментальных результатах. Более того, из экспериментальных данных можно получить лишь одну функцию & набл ( а), в то время как соответствующая спектрофотометрическая функция § ( а) может быть определена для нескольких длин волн. Поэтому лучше всего применение метода следует еграничивать теми системами, для которых можно твердо установить, что только одна из форм ВА или А влияет на кинетику йселедуемой реакции. [30]
Страницы: 1 2 3 4