Определение - концентрация - кислота
Cтраница 3
Таким образом, концентрация изменяется в огромное число раз вблизи точки, при которой количества кислоты и основания эквивалентны. Вследствие этого постепенное добавление основания к кислоте, называемое титрованием, используется в качестве чувствительного метода определения концентрации кислоты. [31]
Метод основан на измерении электропроводимости растворов. Для целей санитарно-химического анализа он может найти дальнейшее развитие при исследовании состава различных солевых растворов, определении концентраций кислот и растворов органических соединений. [32]
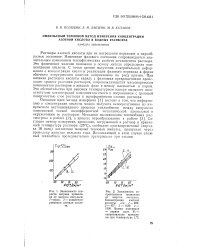
Эти кривые показывают, что зависимость удельной электропроводности от концентрации не является однозначной. Поэтому использование метода измерения электропроводности для определения концентрации кислоты возможно лишь на отдельных восходящих или нисходящих ветвях кривой. [33]
Кинетические результаты обычно выражают в терминах концентрации реагентов. Это не представляет трудностей, если кислотно или основно катализируемые реакции изучают в присутствии известных концентраций добавленной кислоты или иона гидроксила. Однако измерения скорости с применением для определения концентрации кислоты или основания значений рН приводят к константам скорости для кислотно или основно катализируемых реакций, основанным на активностях, а не на концентрациях реагентов. [34]
Растворы азотной кислоты при их нагревании переходят в парообразное состояние. Изменение фазового состояния сопровождается значительным изменением теплофизических свойств компонентов раствора. Это физическое явление положено в основу метода определения концентрации кислоты. С точки зрения получения измерительной информации о концентрации кислоты реализация фазового перехода в форме О бычиого непрерывного кипения неприемлемо по ряду причин. При кипении растворов кислоты наряду с фазовыми превращениями происходит процесс разгонки растворов, сопровождающийся массопереносом компонентов растворов в жидкой фазе и между жидкостью и паром. Это обстоятельство при высоком температурном напоре вызывает несоответствие концентраций компонентов смеси в пограничном с греющей поверхностью слое раствора и периферийными слоями раствора. [36]
 |
Установка для потен-циометрического титрования. [37] |
Вторая часть работы состоит в титровании смеси кислот или многоосновной кислоты. Для этой цели может быть взята смесь соляной и уксусной кислот. Вместо последней может быть использована также фосфорная или хромовая кислота. Выполнение работы завершается определением концентрации кислоты или смеси кислот контрольного раствора. [38]
Электролиз ведут в течение одного часа. Выключив ток, открывают кран в электролитическом ключе и дают стечь содержимому в оба стакана. Вынимая ключ и катод, также дают возможность стечь с них раствору. Катодный стакан снова взвешивается с кислотой с точностью до 0 01 г. Определяют вес катодной жидкости. Для определения концентрации кислоты после опыта снова проводят титрование. Зная титр и объем щелочи, пошедший на титрование кислоты до опыта и после него, а также общее количество кислоты, можно рассчитать изменение количества ионов водорода в катодном пространстве. Кулонометр дает общее количество электричества Q, протекшее по цепи - за время электролиза. [39]
Электролиз ведут в течение одного часа. Затем, выключив ток, открывают кран в электролитическом ключе. Вынимая ключ и катод, дают возможность стечь с них раствору. Катодный стакан снова взвешивается с кислотой с точностью до 0 01 г. Определяют вес катодной жидкости. Для определения концентрации кислоты после опыта снова проводят титрование. Зная титр и объем щелочи, пошедший на титрование кислоты до опыта и после него, а также общее количество кислоты, можно рассчитать изменение количества ионов водорода в катодном пространстве. Кулонометр дает общее количество электричества Q, протекшее в цепи за время электролиза. [40]
Хорошо известно, что производные феназина дают удивительные окраски в концентрированной серной кислоте и что эти растворы изменяют цвет при постепенном разбавлении их водой. Керман [128] высказал предположение, что изменения цвета соответствуют образованию моно -, ди - и триселей с кислотой, так как число определенных цветовых фаз всегда равно числу атомов азота в феназине. Керман считал, что если бы у ряда солей наблюдалось непрерывное изменение поглощения в сторону больших длин волн, то в таком случае можно было бы допустить, что структуры всех этих солей имеют одинаковую природу. Однако если, например, моносоль поглощаете области более коротких волн, чем основание или ди - и трисоли, то тогда структура моносоли должна быть отличной и иметь, вероятно, о-хиноидное строение, так как охиноидный хромофор поглощает обычно в области более коротких волн. Изучение спектров поглощения было проведено со спектрометром с недостаточной разрешающей способностью [132], и различные соли были идентифицированы только определением концентрации кислоты. Тем не менее область каждого максимума поглощения была достаточно хорошо очерчена. [41]
Страницы: 1 2 3