Определение - коэффициент - активность - электролит
Cтраница 1
Определение коэффициентов активности электролитов в смешанных растворах двух электролитов с общим ионом чаще всего производится путем измерения активности растворителя с последующим использованием уравнения Гиббса - Дюгема. [1]
При определении коэффициентов активности электролитов возникают осложнения. [2]
Обычно при определении коэффициентов активности электролитов экспериментально измеренные активности относятся ко всей брутто концентрации электролита. При таком приеме стандартизации неполная диссоциация сказывается в значительном снижении коэффициентов активности ионов таких электролитов. [3]
Обычно при определении коэффициентов активности электролитов экспериментально измеренные активности относятся ко всей брутто концентрации электролита. При этом неполная диссоциация сказывается в значительном снижении коэффициентов активности ионов таких электролитов. Если отнести экспериментально определенные активности к истинной концентрации ионов, то получаются так называемые ионные коэффициенты активности, величина которых не зависит от степени диссоциации. Подробно эти соотношения рассматриваются в гл. [4]
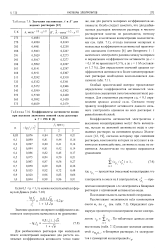 |
Значения постоянных А и В для водных растворов [ 12.| Коэффициенты активности ионов. [5] |
Особый практический интерес представляет определение коэффициентов активностей электролитов в смешанных ( многокомпонентных) растворах. Для смешанных растворов с и, 0 1 справедливо правило ионной силы. Согласно этому правилу коэффициент активности данного сильного электролита одинаков во всех растворах с равной ионной силой. [6]
Применение новых типов ионоселективных электродов для термодинамического исследования многокомпонентных растворов, в частности для определения коэффициентов активности электролитов, может существенно расширить возможности метода ЭДС при изучении водных растворов. [7]
Важную группу составляют элементы без переноса. Такие элементы используются для определения коэффициентов активности электролитов. При этом электроды выбираются так, чтобы один был обратим по катиону, по другой - к аниону исследуемого электролита. [8]
Установлено, что всаливающая способность электролитов по отношению к данному неэлектролиту возрастает вместе с их способностью к экстрагированию. На примере уранилнитрата разработана методика определения коэффициентов активности электролитов в водных растворах методом экстракции. В области термодинамики экстракционных систем получены экспериментальные характеристики экстракционных равновесий, сделаны интересные попытки объяснить наблюдаемые явления, а также внесен ряд усовершенствований в расчетные уравнения. [9]
Установлено, что всаливатощая способность электролитов по отношению к данному неэлектролиту возрастает вместе с их способностью к экстрагированию. На примере уранилнитрата разработана методика определения коэффициентов активности электролитов в водных растворах методом экстракции. В области термодинамики экстракционных систем получены экспериментальные характеристики экстракционных равновесий, сделаны интересные попытки объяснить наблюдаемые явления, а также внесен ряд усовершенствований в расчетные уравнения. [10]
Страницы: 1