Зависимость - растворимость - вещество
Cтраница 2
Кривые, показывающие зависимость растворимости веществ рт температуры, имеют большое практическое значение. С их помощью можно заранее рассчитать количество вещества, которое необходимо взять для приготовления его насыщенного раствора при определенной температуре; так же определять концентрацию насыщенного раствора при данной температуре. [16]
Экспериментальные данные позволяют установить зависимость растворимости вещества в газе от давления вплоть до давлений в несколько тысяч атмосфер. [17]
Это уравнение, выражающее зависимость растворимости вещества в идеальном растворе от температуры, называется уравнением Шредера. Числитель правой части уравнения выражает теплоту плавления чистого компонента при температуре раствора. Поскольку эта величина всегда положительна, растворимость твердого тела в идеальном растворе с повышением температуры возрастает. Если однокомпо-нентная фаза является жидкой, то переход образующего ее компонента в раствор не связан с изменением агрегатного состояния и в случае идеального раствора растворимость, согласно изложенному выше, не зависит от температуры. [18]
Однако подобные диаграммы характеризуют так же зависимость растворимости веществ от температуры. [19]
Политермические способы получения пересыщенных растворов основаны на зависимости растворимости веществ от температуры. Таким образом создается пересыщение. [20]
Уравнение ( II 1.21) показывает, что зависимость растворимости вещества в газе от давления полностью определена зависимостью от давления мольного объема чистого вещества в конденсированном состоянии, а также парциального мольного объем а вещества в его бесконечно разбавленном газовом растворе. [21]
В интервале не очень больших давлений это уравнение качественно верно описывает зависимость растворимости вещества в сжатом газе от давления. При более высоких давлениях даже качественное схождение нарушается. Кривая растворимости, рассчитанная по уравнению ( 6), всегда выпукла к оси давлений. Подсчет величин N по уравнению ( 6) дает величины, значительно более низкие, чем экспериментальные. Объясняется это тем, что при выводе этого уравнения ( точно так же, как это было сделано ранее Дальтоном) не учитывалось наличие сил взаимодействия между молекулами компонентов в газовой фазе. На то, что такое взаимодействие существует, указывает постоянно обнаруживаемая экспериментально зависимость концентрации вещества в газовой фазе не только от температуры и давления, но и от природы газа. [22]
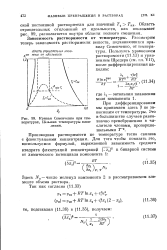 |
Кривая Семенченко при температурах, больших температуры плавления. [23] |
Рассмотрим теперь зависимость растворимости веществ, подчиняющихся правилу Семенченко, от температуры. [24]
Говоря о растворимости вещества, надо указывать, при какой температуре эта растворимость учитывается. Чтобы нагляднее представить зависимость растворимости вещества от температуры, эту зависимость выражают графически. На горизонтальной оси ( оси абсцисс) откладывают температуру, а на вертикальной ( оси ординат) - растворимость. Затем по точкам откладывают величины, выражающие растворимость вещества при разных температурах. Полученные точки соединяют линией, называемой кривой растворимости данного вещества. На рисунке 24 представлена кривая растворимости селитры в воде, а на рисунке 25-кривые растворимости некоторых солей. [25]
Величина растворимости вещества при данных термодинамических условиях и неизменном химическом составе твердой фазы не является однозначной величиной, а зависит от размеров частиц растворенного вещества. Согласно представлениям Оствальда [68], зависимость растворимости вещества от его дисперсности определяется поверхностной энергией частиц. [26]
Неорганические вещества чаще всего кристаллизуют из водных растворов, реже - из спиртовых и водно-спиртовых, а органические вещества - также из растворов в различных органических жидкостях. Метод кристаллизации определяется главным образом характером зависимости растворимости вещества от температуры. В тех случаях, когда растворимость вещества мало изменяется: температурой ( например, NaCl в воде), кристаллизацию производят путем частичного или практически полного удаления растворителя выпариванием раствора. Так как температура кипения насыщенного раствора постоянна, то рассматриваемый метод кристаллизации называется изотермическим. [27]
Зародыши кристаллов самопроизвольно образуются лишь в пересыщенном растворе. На рис. 2 - 1 представлена диаграмма состояний раствора [ 41, с. Пространство между двумя сплошными кривыми характеризует область существования пересыщенного раствора, где он может находиться в псевдоравновесном состоянии достаточно длительное время. Нижняя кривая - зависимость растворимости вещества от температуры. При этом скорость выпадения осадка настолько велика, что образующаяся твердая фаза представлена в основном глобулами аморфного вещества, которые постепенно кристаллизуются в процессе старения осадка. [28]
Страницы: 1 2