Определение - скорость - окисление
Cтраница 1
Определение скорости окисления крайне затруднено благодаря огромному каталитическому влиянию реакции 85 ( см. стр. Оно выражается не столько в отклонении константы скорости окисления, сколько в том, что окисление одного и того же соединения часто протекает с различной скоростью в зависимэсти от качества раствора гидроперекиси бензойной кислоты. Поэтому сравнимые данные можно получить лишь в тех случаях, когда окисление происходит при помощи растворов гидроперекиси, приготовленной в одинаковых условиях. Обычно и этого недостаточно 85, так как оказалось, что даже один и тот же раствор гидроперекиси дает в различное время различные скорости окисления, а именно старые растворы гидроперекиси бензойной кислоты дают иногда большие, иногда меньшие скорости окисления, чем свежеприготовленные растворы. Поэтому, для получения сравнимых результатов необходимо проводить опыты одновременно и с одним и тем же раствором гидроперекиси бензойной кислоты. [1]
Для определения скорости окисления чаще всего пользуются весовым методом благодаря его простоте и универсальности. В простейшем случае он требует только нагревательной печи и точных весов. Существуют различные устройства для взвешивания, но в каждом случае приходится соблюдать определенные предосторожности. [2]
При определении скорости окисления более точные результаты дает определение количества прореагировавшего кислорода - анализируется не окисляемое вещество, а окружающая среда, например, газ. [3]
 |
Простая манометрическая установка [ 4011. [4] |
Манометрические методы определения скорости окисления в принципе очень просты. Установка состоит в основном из нагреваемой трубки-реактора, манометра и приспособления для подачи газа. [5]
Следовательно, для определения скорости окисления окиси азота необходимо знать значение константы скорости прямой реакции и значение константы равновесия реакции диссоциации двуокиси азота. [6]
Таким образом, для определения скорости окисления окна азота необходимо знать значения константы скорости прямо. [7]
Все изложенные в настоящей главе методы определения скорости окисления относятся к изотермическим в том отношении, что ход окисления во времени определяют при нескольких постоянных значениях температуры при том или ином давлении газа. С учетом первостепенной важности температуры в предопределении хода окисления вообще станет ясно, что именно этим путем, бесспорно, можно получить наиболее достоверные и самые подробные сведения. Однако Баур, Бриджес и Фассел [649] предложили неизотермическую методику, которой, по-видимому, присущи те преимущества, что она позволяет составить за короткое время предварительное представление об особенностях окисления в определенных температурных интервалах на ограниченном количестве материала. Этой же методике следовали Кофстад [650] и Спинеди [651], подтвердившие ее изложенные выше преимущества. [8]
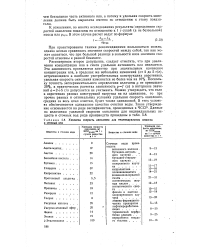 |
Удельная скорость окисления для индивидуальных веществ и сточных вод. [9] |
К сожалению, во многих исследованиях результаты определения скоростей окисления показаны по отношению к 1 г сухой ( а не беззольной) массы ила рсух. [10]
Использование уравнения ( VI, 18) для определения скорости окислений циклогексанона дает удовлетворительный результат только до момента достижений максимума на кинетической кривой циклогексанона. Затем вторичные процессы сильно меняют величину константы скорости. [11]
Для установления предельно допустимой нагрузки на аэротепк и определения скорости окисления гликолевой кислоты поставлены опыты на лабораторном аэротенке-смесителе. [12]
Другой пример, аналогичный окислению олеиновой кислоты, приведен в работе Миттельмана и Пальмера [36] по определению скорости окисления пленок триолеина. Полученные результаты будут более детально обсуждены ниже при рассмотрении предложенного этими авторами способа математического расчета. [13]
Гульбрансен [227] пришел в предварительном порядке к выводу о том, что экстраполяцию результатов кратковременных опытов по определению скорости окисления циркония ( чтобы составить представление о его поведении при длительном окислении) лучше всего делать с помощью кубического уравнения. [14]
При расчете прудов определяют их размеры, обеспечивающие необходимую продолжительность пребывания в них сточных вод. В основе расчета определение скорости окисления, которую оценивают по ВПК и принимают для вещества, разлагающегося наиболее медленно. [15]
Страницы: 1 2