Зависимость - скорость - коррозия - титан
Cтраница 1
Зависимость скорости коррозии титана ВТ1 в 2 % - ном растворе брома в метиловом спирте от величины отрицательного потенциала, поддерживаемого внешней катодной поляризацией. [1]
 |
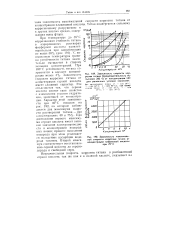
Зависимость скорости коррозии Ti в 40 % - ном растворе H2SO4 от концентрации ионов Ti4 при различных температурах. [2] |
На рис. 3 показана зависимость скорости коррозии титана от концентрации ионов Ti4 и температуры в 40 % - ном растворе серной кислоты. [3]
Выбор методов защиты титана от коррозии в средах, в которых он недостаточно устойчив ( см. главу I), должен быть, по нашему мнению, основан на изучении зависимости скорости коррозии титана от его электродного потенциала. [4]
С по-вышением температуры граница устойчивости титана значительно смещается в сторону меньших концентраций. Зависимость скорости коррозии титана от концентрации серной кислоты имеет сложный характер. Это объясняется тем, что серная кислота меняет свои свойства с изменением степени гидратации, зависящей от концентрации. При достижении первого максимума серная кислота имеет высокие значения электропроводности и концентрации водородных ионов; процесс выделения водорода при этом усиливается вследствие адсорбции водорода титаном. Второй максимум соответствует восстановлению серной кислоты до сероводорода и свободной серы. [6]
Растворы фосфорной кислоты оказывали менее агрессивное действие как на титан, так и на его сплавы с хромом, чем растворы серной и соляной кислот. Зависимости скорости коррозии титана и его сплава с 9 % хрома от потенциала в 7296-ном растворе фосфорной кислоты при 60 С почти одинаковы. [7]
 |
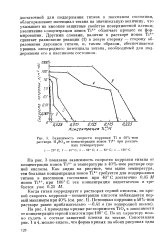
Зависимость Екор титана от концентрации Ti ( IV-ионов в кипящих растворах HNOs различных концентраций ( моль / л. [8] |
Титан обладает высокой коррозионной стойкостью в азотной кислоте ( рис. 3.1) и во многих азотнокислых средах. Зависимость скорости коррозии титана от концентрации кипящих растворов HNO3 приведена на рис. 3.2. Результаты коррозионных испытаний титана в растворах азотной кислоты по данным разных авторов довольно значительно различаются между собой, что объясняется, во-первых, разными условиями испытаний и, во-вторых, большим влиянием на скорость коррозии титана примесей, имеющихся или попадающих при испытаниях в кислоту. [9]
Исследования, результаты которых приводятся ниже, касаются коррозионного и электрохимического поведения сплавов системы титан - молибден, а также нелегированных титана [32-34] и молибдена в растворах едкого кали при концентрациях от 40 до 50 % и температурах 100 - 150 С. На рис. 8 представлена зависимость скорости коррозии титана от потенциала, полученная в 50 % - ном растворе едкого кали. На потенциостатичееких кривых 1 и 2 имеются явно выраженные области активного растворения титана с максимумами при потенциале пассивации, равном - 0 7 в. Повышение концентрации щелочи увеличивает скорость коррозии титана. По сравнению с растворами кислот в щелочных растворах активная область растворения титана смещена к более отрицательным значениям потенциала. [10]
Для сравнения на этом же графике приведена кривая для атмосферы воздуха. На фигуре видно, что общий вид зависимости скорости коррозии титана от концентрации серной кислоты, полученной для атмосферы воздуха, сохраняется и для других атмосфер. В одной из предыдущих наших работ [4 ] было показано, что кислород играет основную роль в пассивации титана в разбавленных растворах серной кислоты. [11]
Титан химически нестоек в растворах серной кислоты. При повышении концентрации серной кислоты и температуры скорость коррозии титана возрастает. На рис. 3.7 представлена зависимость скорости коррозии титана от концентрации серной кислоты. [12]
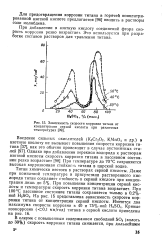 |
Зависимость скорости коррозии титана от концентра-ции серной кислоты при различных температурах. [13] |
Титан химически нестоек в растворах серной кислоты. При повышении концентрации серной кислоты и температуры скорость коррозии титана возрастает. На рис. 15 представлена зависимость скорости коррозии титана от концентрации серной кислоты. [14]
Титан химически не устойчив в растворах серной кислоты. При повышении концентрации серной кислоты и температуры скорость коррозии титана возрастает. При 100 пассивное состояние титана сохраняется только в 0 2 -ной серной кислоте. На рис. I представлена зависимость скорости коррозии титана от концентрации серной кислоты. [15]
Страницы: 1