Зависимость - скорость - обмен
Cтраница 2
Чтобы выяснить, имеется ли в данном случае простое каталитическое действие отрицательных ионов или же явление мостичного переноса, следует установить характер зависимости скорости обмена от концентрации аниона. [16]
Более подробно нами с участием Г. А. Блоха с сотрудниками, а также А. Ф. Рекашевой и Л. Е. Бурксер изучен обмен в связях C-S дитиокислот, тиомочевины, 2-меркаптобензтиазола, их производных и аналогов. В табл. 5 показана зависимость скорости обмена от строения в сравнимых условиях. Существенно отметить, что в тех же условиях обмен отсутствует в связях С - S - С. [17]
При изучении явлений изотопного обмена в комплексных соединениях были сделаны наблюдения относительно того, что в отдельных случаях наблюдалась явно выраженная зависимость скорости реакций от освещения. Далее, в работе Рича и Таубе [63] установлена зависимость скорости обмена в хлористых комплексах платины от присутствия следов окислителей и восстановителей, а в работе Дрейера [129] - зависимость скорости изотопного обмена в кислых растворах K2PtCle и K2PtBre как от освещения, так и от следов присутствующих в растворе примесей. [18]
По другим представлениям [853, 854], более распространенным в новых работах, где кикетика изучалась подробнее, переносчиками электронов служат ионы, атомы или радикалы. В ряде случаев участие в переносе продуктов присоединения или гидролиза количественно объясняет зависимость скорости обмена от рН и от концентрации посторонних ионов. С этих точек зрения ускорение ионами хлора обмена Fe4 1 с Fe можно объяснить тем, что в обмене участвуют не эти ионы, a FeCl, FeCl. Эти ионы отдают ионам Fe 1 1 гидроксил вместе с электроном. Следует отметить, что этим представлениям не противоречит рассмотренная выше возможность обмена через промежуточные комплексы. [19]
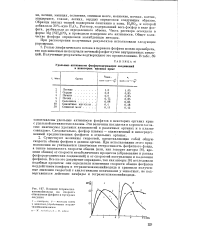 |
Влияние тетрамотил-аммонийиодида на скорость обновления фосфата в мускулах лягушки. [20] |
Существуют величины скоростей, представляющие собой общую скорость обмена фосфата в данном органе. При использовании этого предположения не учитывается химическая гетерогенность фосфатного фонда, а также зависимость скорости обмена ( или, как говорят авторы [8], времени обмена) от скорости метаболических процессов ( образование и распад фосфорорганических соединений) и от скоростей поступления и выделения фосфатов. Все же это допущение оправдано, так как авторы [8] исследовали подобные процессы: они определили изменения скорости обмена фосфатов под действием камфары и тетраметиламмонийиодида и сравнили полученные значения скоростей с аналогичными величинами у животных, не подвергавшихся действию камфары и тетраметиламмонийиодида. [21]
При выяснении вопроса об определяющем в ионообменной кинетике значении химического или диффузионного механизмов наиболее наглядным показателем являются результаты, полученные при изучении зависимости скорости процессов ионного обмена от зернения сорбента. Действительно, если скорость-определяющей стадией является химическая реакция, то кинетика процесса не будет зависеть от величины зерен сорбента; наоборот, зависимость скорости обмена от зернения сорбента однозначно свидетельствует о решающей роли одного из диффузионных процессов. [22]
Например, минеральный катионит шабазит, доступные обменные точки которого расположены внутри небольших пор, дает только очень малые скорости обмена. В противоположность шабазиту на каолините-глинистом материале, обменные точки которого расположены на поверхности и на ребрах пластинчатых чешуек, ионы обмениваются почти мгновенно. Зависимость скорости обмена от геометрического расположения обменных точек в ионите была подтверждена и дальнейшими исследованиями. [23]
Добавление трихлоруксусной кислоты ( ТХУК) или триэтил-амина ( ТЭА) к раствору - оксибензойной кислоты в ДМСО вызывает сужение сигнала, указывающее на ускорение обмена. На рис. 3 приведены спектры, показывающие влияние ТХУК на ширину слитого сигнала. Зависимость скорости обмена в 2-мол. Кислота катализирует обмен сильнее, чем щелочь. [24]
Это явление В. А. Плесков и Н. Б. Миллер объясняют ослаблением связи между ионами цинка и анионами SCU2 и ОН - у высших аммиакатов. При введении в раствор избытка ионов SO42 - скорость обмена уменьшается. Кроме того, зависимость скорости обмена от концентрации цинка значительно ослабляется в растворах аммиакатов. [25]
Какой же из этих механизмов является определяющим в ионообменной кинетике. Ответ на этот вопрос может быть получен из опытов по определению скорости процесса на ионите с различным размером его зерен. Если скорость процесса не зависит от размера зерна ионита, то лимитирующей стадией является химическая кинетика. Зависимость скорости обмена от размера зерен ионита указывает на решающую роль одного из диффузионных процессов. Поставив опыты по изучению зависимости скорости обмена от скорости перемешивания ( статические условия) либо от скорости пропускания раствора ( динамические условия) на ионитах с одинаковым временем контакта, можно установить, какой из диффузионных процессов ( гелевый или пленочный) имеет решающее значение. Изменение скорости обмена от скорости перемешивания или пропускания раствора указывает на определяющую роль пленочной кинетики. [26]
Каталитические свойства индивидуальных комплексов с переносом заряда обнаружены на примере активности КПЗ аминов с тетрагалоидхинонами в реакции орто-пара-превращения водорода. КПЗ фталоцианинов различных металлов с натрием в реакциях дейтероводо-родного обмена, изомеризации бутена и гидрогенизации олефинов, причем в таких условиях, в которых исходные фталоцианины в отсутствие натрия этих реакций не ведут. Заметную активность в реакции Н2 - Е) 2-обме-на проявляют также комплексы натрия со многими ароматическими углеводородами. Для этих комплексов обнаружена зависимость скорости обмена от сродства к электрону акцепторного компонента, имеющая экстремальный характер. [27]
Какой же из этих механизмов является определяющим в ионообменной кинетике. Ответ на этот вопрос может быть получен из опытов по определению скорости процесса на ионите с различным размером его зерен. Если скорость процесса не зависит от размера зерна ионита, то лимитирующей стадией является химическая кинетика. Зависимость скорости обмена от размера зерен ионита указывает на решающую роль одного из диффузионных процессов. Поставив опыты по изучению зависимости скорости обмена от скорости перемешивания ( статические условия) либо от скорости пропускания раствора ( динамические условия) на ионитах с одинаковым временем контакта, можно установить, какой из диффузионных процессов ( гелевый или пленочный) имеет решающее значение. Изменение скорости обмена от скорости перемешивания или пропускания раствора указывает на определяющую роль пленочной кинетики. [28]
В этой реакции могут принимать участие молекулы фенола и воды, а также гидро-ксильный и фенолятный ионы. Реакция между ОН - и C6HsO - должна ускоряться с ростом концентрации основания. Реакции между ОН - и С6Н5ОН и между Н2О и СеН50 - также должны ускоряться с ростом концентрации основания, однако только до тех пор, пока по следняя не сделается равной концентрации фенола; дальнейшее увеличение концентрации основания не должно приводить к ускорению обмена. Наконец, скорость реакции Н2О с С6Н5ОН не должна зависеть от концентра-ции основания. Было найдено, что скорость обмена достигает максимума при концентрации основания, равной половине концентрации фенола. Эти данные согласуются лишь с тем, что участниками обмена являются молекулы фенола и фенолятные ионы: первые в качестве донора, а вторые - в качестве акцептора дейтерия. Только в этом случае понятна зависимость скорости обмена от концентрации основания: когда последняя равна половине концентрации фенола, в системе присутствует одинаковое количество доноров и акцепторов и скорость максимальна. Реакция между фенолятными ионами и молекулами воды также имеет место, но протекает значительно медленней, так как вода - более слабая кислота, чем фенол. [29]
Страницы: 1 2