Зависимость - скорость - превращение
Cтраница 1
 |
Зависимость константы скорости А окисления SO2 от температуры Гв кинетической области ( / и на промышленном зерне катализатора ( 2. [1] |
Зависимость скорости превращения от температуры характерна для обратимой реакции ( см. разд. [2]
Зависимость скорости превращения или скорости реакции от условий ее протекания называют кинетическим уравнением или кинетической моделью реакции. [3]
 |
Зависимость константы скорости k окисления SO2 от темпе-ратуры Т в кинетической области на мелком зерне катализатора ( / и на промышленном зерне катализатора. [4] |
Зависимость скорости превращения от температуры характерна для обратимой реакции - ( см. разд. [5]
Уравнения, описывающие зависимость скорости превращения веществ или реакции от концентраций реагентов, температуры, давления, состояния катализатора и других воздействий на них, называют кинетической моделью реакции, или кинетическими уравнениями. [6]
Предполагалось, что известна зависимость скорости превращения от температуры, давления и состава реагирующей смеси. При этом нас не интересовало, является ли реакция процессом, протекающим однородно во всей системе, или наблюдаемая степень превращения складывается из множества отдельных независимых микропроцессов. [7]
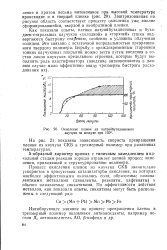 |
Окисление пленок из натрийбутадиенового каучука на воздухе при 150. [8] |
На рис. 21 показана зависимость скорости превращения пленки из каучука СКВ в трехмерный полимер при различных температурах. [9]
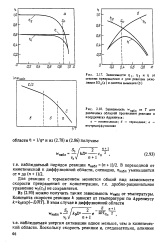 |
Зависимости щ, т 2 и Г от степени превращения х для реакции окисления SO 2 ( а и синтеза аммиака ( б.| Зависимость wHS6n от Т для различных областей протекания реакции в координатах Аррениуса. [10] |
Для реакции с торможением меняется общий вид зависимости скорости превращения от концентрации, т.е. дробно-рациональное уравнение wn ( cn) не сохраняется. [11]
Вторым весьма интересным эффектом, к которому приводит конвекция, является зависимость скорости превращения от ориентации реакционного сосуда в пространстве. Особенно заметен должен быть этот эффект для плоскопараллельных сосудов. Если расположить боковую поверхность такого сосуда горизонтально, то при малой высоте сосуда конвекция может быть весьма мала. Таким образом, меняя положение сосуда в пространстве, можно изучить роль конвекции. [12]
Певзнер, Т.Д. Кубьгшкиной и автора [128], проведенными на стабилизированном аустените, было показано, что после переохлаждения до температур - 5и - - 16tTC превраще нияГ аустенита в мартенсит происходят изотермически и начинаются после некоторого инкубационного периода. Зависимость скорости превращения от времени изотермической выдержки характеризуется кривой с максимумом. [13]
 |
Свойства эфиров этилфенилфосфинистой кислоты. [14] |
На рисунке приведены изотермы скорости реакции указанных фосфористых эфиров с четыреххлористым углеродом. График зависимости скорости превращения от времени изображается S-образной кривой. В случае триметил - и трибутилфосфитов изгиб кривой носит явно выраженный ступенчатый характер. По-видимому, такой ход кривой скорости реакции объясняется радикально-цепным механизмом реакции. Если нижний горизонтальный участок на кривой соответствует периоду инициирования цепи, второй вертикальный участок - ее росту и, наконец, третий - периоду обрыва цепи. [15]
Страницы: 1 2