Определение - теплота - растворение
Cтраница 2
Определение теплоты гидратообразования сводится к определению теплот растворения безводной соли и ее кристаллогидрата. Берут две навески по 7 5 г растертого в порошок кристаллогидрата. Первую навеску используют для определения теплоты растворения кристаллогидрата, а вторую переносят в фарфоровую чашку и нагревают на горелке до тех пор, пока не получится порошок безводной соли. Пересыпают ее в предварительно взвешенную пробирку, которую сейчас же закрывают резиновой пробкой, и после остывания пробирку взвешивают. Производят определение теплоты растворения безводной соли в 300 г, а кристаллогидрата в 297 г воды. [16]
В табл. 1 приведены результаты опытов по определению теплоты растворения КС1 в воде при разведении 1: 450 и температурах 25, 15, 10 С. [17]
 |
К расчету теплоты растворения марганца в жидком кремнии ( при 1470. [18] |
Рассмотрим результаты опыта № 3, посвященного определению теплоты растворения железа в жидком кремнии. [19]
Работа состоит из трех частей: 1) определение теплоты растворения карбамида ДЯт; 2) построение диаграммы плавкости системы CO ( NH2h - Н2О: а) по расчету с использованием значения ДЯ, и уравнения ( VI. [20]
Определение теплоты образования кристаллогидрата, которое сводится к определению теплот растворения безводной соли и ее кристаллогидрата. [21]
Основными методами, позволяющими оценивать плотность упаковки цепей полимеров, являются методы определения теплот растворения и изотерм сорбции. В работе [2] было показано, что сорбционная способность целлюлозы при малых значениях относительной влажности значительно больше, чем у стеклообразной глюкозы. Это обстоятельство авторы объясняют тем, что целлюлоза вследствие большой длины ее молекул обладает рыхлой упаковкой. [22]
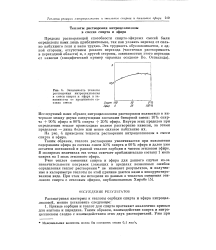 |
Зависимость теплоты растворения нитроцеллюлозы в смеси спирта и эфира в зависимости от процентного состава смеси. [23] |
Учет теплот смешения спирта и эфира для данного случая из-за незначительности поправок ( лежащих в пределах возможных ошибок определения теплот растворения не изменяет результатов, и полученные в калориметре теплоты по этой причине даются нами в некорректированном виде. [24]
 |
Термодинамические характеристики процесса. [25] |
В связи с этим для расчета теплоты образования безводного фосфата празеодима нами был использован метод, основанный на определении теплоты растворения труднорастворимой соли. [26]
После завершения работы над материалами настоящей главы была опубликована работа Ганна и Грина [1887], в которой было выполнено еще одно определение теплоты растворения металлического лития в воде. [27]
Из других работ физико-химического характера, связанных с изучением поливинилхлорида, представляют интерес исследования Липатова, Каргина и Слонимского [281], связанные с определением теплот растворения и изучением сорбции паров ориентированными и неориентированными пленками полимера, исследования Фицджералда, Миллера [282], Фанта и Сазер-ленда [283], Менара и Эро [284], Кайона [285], Ферри и Фицджералда [286], посвященные изучению диэлектрических свойств поливинилхлорида, и работа Олфорда и Дола [287] по определению зависимости удельной теплоемкости ( Ср) от температуры. [28]
Значение теплоты образования Со ( НС02) 2 довольно хорошо совпадает со значением, найденным Ерофеевым [136] по теплоте растворения этой соли ( автор не указывает метода определения теплоты растворения), а значение Д / / 298 - 77 ккал для Cd ( N03) 2 ( K), приведенное Биховским и Россини как сомнительное, явно не соответствует действительности. [29]
Сомнительным становится само существование твердого раствора NaF и Na2SiF6, если не полагать, что малая растворимость Na2SiFe приводила, вопреки утверждению Хантке, к систематическим ошибкам определения теплоты растворения сплава. [30]
Страницы: 1 2 3 4