Определение - условие - равновесие
Cтраница 1
Определение условий равновесия минимизацией значений энергии Гиббса - процедура во многих случаях трудоемкая по сравнению с другими методиками расчетов испарения, приведенными в этой главе. Для бинарных смесей нет необходимости применять множители Лагранжа, так как энергия Гиббса смеси обычно выражается исходя из единственного молярного состава. Это обстоятельство учитывается в примере 6.11. Примеры методик с использованием множителей Лагранжа подробно описаны в гл. [1]
Определение условий равновесия связано с нахождением максимальной работы химической реакции. [2]
Определение условий равновесия в испарителе ( цикл 5) имеет следующие особенности. [3]
Для определения условий равновесия применяют различные модификации приведенных выше уравнений. [4]
Для определения условий равновесия между окислами азота и раствором азотной кислоты с различными добавками нет надобности в непосредственном экспериментальном определении равновесного состава окислов азота над раствором. [5]
Для определения условий газожидкостного равновесия используются законы Рауля и Дальтона, согласно которым константа равновесия характеризуется отношением молярных долей компонента в равновесных газовой и жидкой фазах или отношением парциального давления компонента к общему давлению системы. Отсюда следует, что с увеличением давления системы уменьшается молярная концентрация компонента в газовой фазе при одновременном ее возрастании в жидкой. Температура влияет на процесс в обратном направлении: с повышением температуры растет давление паров ( а следовательно, и молярная концентрация компонента) в газовой фазе при соответственном ее уменьшении в жидкой фазе. [6]
Для определения условий газожидкостного равновесия используются законы Рауля и Дальтона ( см. гл. Отсюда следует, что с увеличением давления системы уменьшается молярная концентрация компонента в газовой фазе при одновременном ее возрастании в жидкой. Температура влияет на процесс в обратном направлении: с повышением температуры растет давление паров ( следовательно, и молярная концентрация компонента) в газовой фазе при соответственном ее уменьшении в жидкой фазе. [7]
Для определения условий газожидкостного равновесия используются законы Рауля и Дальтона, согласно которым константа равновесия характеризуется отношением молярных долей компонента в равновесных газовой и жидкой фазах или отношением парциального давления компонента к общему давлению системы. Отсюда следует, что с увеличением давления системы уменьшается молярная концентрация компонента в газовой фазе при одновременном ее возрастании в жидкой. Температура влияет на процесс в обратном направлении: с повышением температуры растет давление паров ( а следовательно, и молярная концентрация компонентов) в газовой фазе при соответственном ее уменьшении в жидкой фазе. [8]
Помимо определения условий равновесия тела, представляет интерес и вопрос о его устойчивости. [9]
 |
Схема для вывода уравнения равновесного краевого угла в системе жидкость ( ж - твердое тело ( т - газ ( г. [10] |
Для определения условий равновесия фаз при смачивании нужно рассчитывать работу, связанную с изменениями площадей контакта. Из-за влияния адсорбции вывод уравнения равновесного краевого угла для многокомпонентных систем ( например, при смачивании растворами) сравнительно сложен. Поэтому предварительно рассмотрим более простой случай - контакт однокомпонентных фаз. [11]
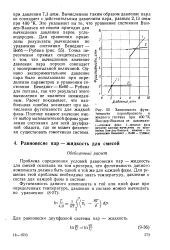 |
Зависимость фугитивности парообразного и жидкого гептана при 400 К Ван-дер - Ваальса от давления. [12] |
Проблема определения условий равновесия пар - жидкость для смесей основана на том критерии, что фугитивность данного, компонента должна быть одной и той же для каждой фазы. Для решения этой проблемы необходимо знать температуру, давление и состав для каждой фазы в системе. [13]
При определении условий равновесия системы твердых тел, находящихся во взаимодействии, задача о равновесии может быть разрешена для каждого тела в отдельности. Силы реакции ( взаимодействия), возникающие в точках соприкосновения, удовлетворяют третьему закону Ньютона. В соответствии с этим мы обязаны принять условие, что действие одного тела на другое равно и противоположно по направлению действию этого другого тела на первое. [14]
Итак, определение условий равновесия системы, включающей малую твердую частицу, представляет для макроскопической термодинамики весьма трудную, до конца не решенную проблему. Опубликованные материалы противоречивы и не свободны от критики. Ситуация усугубляется еще и тем, что к принципиальным трудностям добавляется путаница, которая возникает из-за неправомерного распространения результатов, полученных для частиц, находящихся в равновесии с массивным расплавом или раствором, на изолированные частицы. [15]
Страницы: 1 2 3 4