Определение - электропроводность
Cтраница 2
Определения электропроводности называются кондуктометрическими определениями. Эти определения находят различное применение. [16]
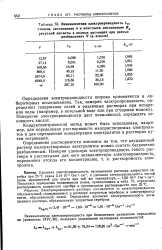 |
Эквивалентная электропроводность Kv. [17] |
Определения электропроводности широко применяются в лабораторных исследованиях. Измерение электропроводности дает возможность определять основность кислот. [18]
Определение электропроводности или удельного электрического сопротивления является значительно более простым с точки зрения его экспериментального выполнения по сравнению с определением теплопроводности, так как установившееся состояние разности потенциалов в двух выбранных точках испытываемого образца достигается практически мгновенно. [19]
Определение электропроводности таких растворов, содержащих элементы иттриевой группы, показало [1, 2], что значительная часть ионов, редкоземельных элементов находится в составе комплексных анионов [ Me111 ( SO4) 3 ] 3 -, что дает основание рассматривать двойные сульфаты как комплексные соединения. Для скандия также установлено [3] образование комплексных анионов в сульфатных растворах, в отличие от алюминия, сульфатные комплексы которого неустойчивы. Это связано, очевидно, с различием в. Но даже для лантана, обладающего из всех лантанидов наименьшей склонностью к образованию комплексных соединений, наблюдается перенос ионов к аноду. [20]
Определение электропроводности, несмотря на ряд известных недостатков, является одним из широко применяемых методов характеристики катализаторов, дающих важную информацию. Определение диэлектрических свойств может также в ряде случаев оказаться полезным. Однако для целей, преследуемых в настоящей работе, измерения электропроводности и функции работы выхода электрона, по-видимому, более целесообразны. В настоящее время в нашей лаборатории проводится определение работы выхода электрона. [21]
Определение электропроводности позволяет найти только сумму подвижностей ионов, составляющих электролит. Между тем в зависимости от природы электролита ток может переноситься в большей или меньшей степени катионами или анионами. В некоторых твердых и расплавленных солях ток переносится только ионами одного знака. Так, в твердой Agl при электролизе двигаются ионы серебра, а в расплавленном РЬС12 - только ионы хлора. В этом растворе часть катионов Zr4 замещена катионами кальция с меньшим зарядом. Условие электронейтральности при таком замещении может сохраниться только благодаря образованию в кристаллической решетке твердого раствора кислородных вакансий. Это означает, что часть узлов решетки, которые в чистом ZrO2 заполнялись ионами О2 - остается пустой. [22]
Определение электропроводности основано на измерении электрического сопротивления раствора. [23]
Определение электропроводности по этому методу основано на использовании мостика Уит-стона. [24]
Определение электропроводности возможно только для противоионов, причем нужно учитывать электроосмотический эффект. [25]
Определение электропроводности раствора является одним из самых простых и точных физических определений. Для определения электропроводности применяются стеклянные сосуды определенной формы и размеров с двумя платиновыми электродами, удерживаемыми в закрепленном положении. Платиновые электроды помрываются платиновой чернью. Затем в сосуд наливается неизвестный раствор, измеряется сопротивление раствора и вычисляется его удельная электропроводность. [26]
 |
Распределение концентрации ионов в межэлектродном пространстве при перемешивании жидкости ( а и в неподвижной жидкости ( б. [27] |
Определение электропроводности электролитов важно с точки зрения количественной оценки степени и константы диссоциации, межионных и других сил в растворе. [28]
Определение электропроводности электролитов состоит из трех основных этапов: калибрования проволоки реохорда, определения постоянной сосуда и измерения сопротивления сосуда, заполненного исследуемым раствором. Кроме того, проводится вспомогательная операция-платинирование электродов. [29]
Определение электропроводности растворов электролитов практически сводится к измерению их сопротивления. Принципиально измерение сопротивления растворов может быть проведено как с помощью постоянного, так и переменного тока. Но в обоих случаях нужно принять особые меры для уменьшения до минимума поляризационного сопротивления. [30]
Страницы: 1 2 3 4