Зависимость - состав - пар
Cтраница 4
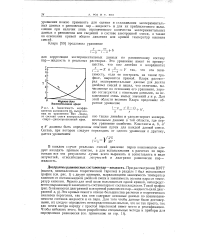
Для систем, в которых зависимость давления пара от состава нелинейна, нет общего выражения, в такой простой форме связывающего составы пара и раствора. Некоторые типичные кривые, выражающие зависимость состава пара от состава раствора в таких системах, показаны на рис. 136 сплошными линиями. Повышение относительного содержания данного компонента в жидкой фазе и здесь вызывает всегда увеличение относительного содержания его в парах. Положительные отклонения давления пара обусловливают образование вогнутости в верхней части кривых, а отрицательные - в нижней их части. [46]
Установил ( 1911) законы, выражающие зависимость состава пара раствора от теплоты испарения его компонентов и темп-ры ( законы В. [47]
Все эти линии состоят из отдельных участков, каждый из которых соответствует определенному трехфазному равновесию, реализуемому в системе. Так, например, линии АВ и АВ дают зависимость состава пара и расплава от температуры при трехфазном равновесии кристаллы KF расплав насыщенный пар, а линия А В - изменение общего давления от температуры при этом равновесии. [48]
Мы сочли необходимым особенно подробно остановиться на значении физико-химического фактора в уравнении ( I-5), так как игнорирование его приводит к неправильным формулировкам первого закона Вревского. В литературе встречаются такие формулировки закона Вревского, в которых зависимость состава пара растворов от температуры определяется соотношением теплот испарения компонентов. В некоторых случаях такая трактовка закона Вревского приводит к неправильным выводам. Поэтому следует придерживаться той формулировки первого закона, которая вытекает из уравнения ( I-5) и которая дана самим Вревским. Для практических целей эта формулировка может быть изложена иначе, принимая во внимание, что сообщение тепла раствору определенной концентрации возможно только при повышении давления в системе. [49]
 |
Зависимость коэффициентов активности ( f, вычисленных по уравнению Ван Лаара, от состава смеси изопропиловый спирт-диизопропиловый эфир. [50] |
При рассмотрении ВЭТГ ( высота, эквивалентная теоретической тарелке) в разделе 1 был использован график ( см. рис. 1) с двумя кривыми, выражающими зависимость температур кипения от состава жидкой двойной смеси и зависимость состава пара от температур кипения. Можно для этой цели пользоваться одной кривой, непосредственно выражающей зависимость состава пара от состава жидкости. [51]
Эксперимент подобен описанному в Работе 2, но с той разницей, что к прибору однократного испарения через шланги, присоединенные к обоим холодильникам, подключают маностат. Равновесие жидкость - пар в бинарной системе исследуют при двух или трех давлениях, включая атмосферное. По графикам зависимости состава пара от состава раствора определяют смещение положения точки состава азеотропа. [52]
Мвр равен сумме моментов всех действующих на тело сил относительно оси вращения и связан с угловым ускорением тела е равенством Мвр It, где / - момент инерции тела относительно оси вращения. Происходит неравномерно: под влиянием гл. Установил ( 1911) законы, выражающие зависимость состава пара раствора от теплоты испарения его компонентов и темп-ры ( законы В. [53]
При рассмотрении ВЭТГ ( высота, эквивалентная теоретической тарелке) в разделе 1 был использован график ( см. рис. 1) с двумя кривыми, выражающими зависимость температур кипения от состава жидкой двойной смеси и зависимость состава пара от температур кипения. Можно для этой цели пользоваться одной кривой, непосредственно выражающей зависимость состава пара от состава жидкости. [54]
При исследовании диаграмм равновесия жидкость - пар их можно представить в виде некоторых полей, заданных в концентрационном симплексе. Например, изобарической диаграмме будут отвечать скалярные поля температур кипения и конденсация, а также поле отрезков, образованное йодами. При этом условии поле нод представляет собой векторное поле, описывающее зависимость состава пара от состава раствора. Поле нод является в то же время полем направлений для дистил-ляционных линий, которые, в свою очередь, служат векторными линиями поля. [55]
Рассмотренные выше уравнения дают необходимую основу для исследования процессов открытого испарения. Один из возможных путей при этом состоит в прямом интегрировании системы ( II. Такой путь может быть использован в конкретных задачах, однако в общем случае он не является вполне удовлетворительным. Зависимость состава пар-а от состава раствора для разных многокомпонентных систем имеет самый разнообразный и зачастую сложный характер. В результате для системы уравнений ( 11 3) может оказаться возможным лишь численное интегрирование. Кроме того, интегрирование в каждом отдельном случае не заменяет исследования общих закономерностей. Отметим также, что практически при разработке новых схем разделения для многокомпонентных смесей часто нет полных данных о зависимости состава пара от состава раствора. [56]
Страницы: 1 2 3 4