Точное определение - точка - эквивалентность
Cтраница 1
Точное определение точки эквивалентности ( появление слабой МУТИ) требует от аналитика определенного навыка. Значительно легче уловить конец титрования, если за колбой поместить черный экран и направить на колбу луч света. [1]
Точное определение точки эквивалентности ( появление слабой мути) требует от аналитика определенного навыка. Значительно легче уловить конец титрования, если за колбой поместить черный экран и направить на колбу луч света. [2]
Таким образом, точное определение точки эквивалентности бывает иногда затруднительно. Чтобы устранить это, предварительно отфильтровывают осадок хлорида серебра, а затем фильтрат вместе с промывными водами титруют раствором роданида калия. [3]
Кривая потенциометрического титрования необходима для точного определения точки эквивалентности и затем расхода рабочего раствора. Во многих технических анализах, где в точке эквивалентности потенциал резко меняется, расход рабочего раствора можно определить, не прибегая к построению графика. [5]
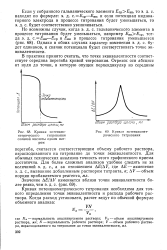 |
Кривая потенциомет-рического титрования.| Кривая потенцио. [6] |
Кривая потенциометрического титрования необходима для точного определения точки эквивалентности и расхода рабочего раствора. [7]
Титрование проводится не менее трех раз при различном разбавлении фильтрата бурового раствора. Если возникают трудности в точном определении точки эквивалентности, то производят различное разбавление в зависимости от нахождения точки эквивалентности. Если она находится в начале титрования ( до 3 мл СаС12), то необходимо уменьшить разбавление, если же она находится при большем вводе хлористого кальция ( более 10 мл), то необходимо увеличить разбавление. [8]
В приведенном выше кратком обзоре различные методы определения элементов указаны лишь схематично. Естественно, что - ляя выполнения этих определений требуется подробное знание сущности происходящих реакций, условий количественного их течения и, особенно, условий точного определения точки эквивалентности титрования. [9]
Точность, достигаемая в реакциях осаждения, зависит от растворимости осадка. Если продукт реакции заметно растворим, то угол наклона кривой около точки эквивалентности будет мал. Вследствие этого будет затруднительно и точное определение точки эквивалентности. [10]
Точность, достигаемая в реакциях осаждения, зависит от растворимости осадка. Если продукт реакции заметно растворим, то угол наклона кривой около точки эквивалентности будет мал. Вследствие этого будет затруднительно и точное определение точки эквивалентности. [11]
 |
Значение константы К. [12] |
Точкой эквивалентности называется момент, когда в раствор А прибавлено столько соединения В, сколько требуется теоретически для реакции с веществом А. Если реакция проходит количественно, то в точке эквивалентности свободного вещества А не должно оставаться. Но те реакции, с которыми имеют дело, обычно проходят не полностью и некоторое количество вещества А остается непрореагировавшим в точке эквивалентности и даже после прохождения этой точки. Мы говорим, что реакция в данных экспериментальных условиях проходит количественно до 1 %, если в точке эквивалентности остается вещество А в количестве 1 % от первоначального его содержания. Обычно, чем ближе реакция к количественному ее прохождению, тем легче точно определить точку эквивалентности. Однако в современных инструментальных методах анализа точные определения точки эквивалентности проводятся и при использовании реакций, проходящих далеко не количественно. [13]
Точкой эквивалентности называется момент, когда в раствор А прибавлено столько соединения В, сколько требуется теоретически для реакции с веществом А. Если реакция проходит количественно, то в - точке эквивалентности свободного вещества А не должно оставаться. Но те реакции, с которыми имеют дело, обычно проходят не полностью и некоторое количество вещества А остается непрореагировавшим в точке эквивалентности и даже после прохождения этой точки. Мы говорим, что реакция в данных экспериментальных условиях проходит количественно до 1 %, если в точке эквивалентности остается вещество А в количестве 1 % от первоначального его содержания. Обычно, чем ближе реакция к количественному ее прохождению, тем легче точно определить точку эквивалентности. Однако в современных инструментальных методах анализа точные определения точки эквивалентности проводятся и при использовании реакций, проходящих далеко не количественно. [14]
Страницы: 1
