Зависимость - сродство
Cтраница 1
Зависимость сродства к электрону от порядкового номера не так проста, как соответствующая зависимость потенциала ионизации. [1]
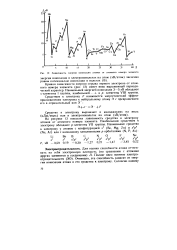 |
Зависимость энергии ионизации атомон от атомного номера элемента. [2] |
На рисунке 13 показана зависимость сродства к электрону атомов от атомного номера элемента. Наибольшим сродством к электрону обладают р-элементы VII группы. [3]
В статье [544] рассматривается зависимость сродства от - степени копланарности молекул нафтохиноновых красителей. [4]
На рис. 19.3 построен график зависимости сродства к электрону от заряда ядра, из которого видно, что в отличие от эндотермического эффекта ионизации сродство к электрону Е может иметь разные знаки. [5]
Таким образом, есть достаточные основания полагать, что зависимость фермент-субстратного сродства от температуры определяется рядом различных механизмов. И в самом деле, иначе трудно было бы объяснить сложную, U-образную форму кривых этой зависимости, полученных для некоторых ферментов. [6]
Эффект Бора, свойственный НЬ, но не Mb, состоит в зависимости сродства НЬ к 02 от рН среды. [7]
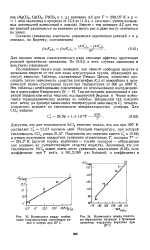 |
Взаимосвязь между изобарными теплоемкостями галогеиидов калия и натрия при 25 С.| Взаимосвязь между теплота-ми образования хлоридов и бромидов, элементов подгруппы бериллия при 25 С. [8] |
Исследования такого рода освещают, как зависят свободные энергии и энтальпии веществ от тех или иных структурных групп, образующих молекулу вещества. Таблицы, составленные Ремоло Циола, позволяют проследить такую зависимость сродства ( логарифма КР) от важнейших в органической химии структурных групп при температурах от 300 до 1000 К. Там же изложен дополненный и развитый Введенским метод чешских исследователей Эрдеша и Черни вычисления термодинамических величин по подобию. Введенский так поясняет этот метод на примере вычисления температурной зависимости С р четырех-хлористого кремния по теплоемкости четыреххлористого углерода. [9]
 |
Некоторые свойства галогенов. [10] |
Аномально низкая энергия диссоциации связи F-F обычно объясняется отталкиванием неподеленных электронов валентных оболочек двух атомов. Экстраполяция зависимости энергии диссоциации молекулы галогена Х2 от 1 / R ( где R - длина связи X-X) дает значение для фтора на - 226 кДж / моль более высокое, чем приведенное в табл. 9.1. Было высказано мнение [2], что аналогичные количественные аномалии возникают и при участии только одного атома фтора. Например, зависимость сродства к электрону от потенциала ионизации для иода, брома и хлора является линейной, а при экстраполяции на фтор дает величину на 1 14 эВ ( 108 8 кДж / моль) большую, чем наблюдаемая. Сходные отклонения наблюдаются для энергии диссоциации ковалентных молекул типа НХ или СН3Х или молекул галогенидов щелочных металлов ( в газообразном состоянии), связь в которых является ионной. [11]
Точно в таком же положении находится водород водяного остатка НО к углероду ц водороду мефила. Здесь сам собою возникает вопрос: в каком отношении находится характер элементов к другим паям, связанным с ними только посредственно; другими словами, зависит ли качество сродства одного многоатомного элемента от качества сродства других паев, находящихся к нему в посредственном отношении. Очевидно, что этот вопрос сводится к вопросу о зависимости сродства свободного и связанного, которые были иояснены примерами окиси углерода и охлоренного углеводородного соединения. Мефильный алкоголь представляет только более сложный случай того же рода. Сложность обусловливается тем, что здесь входят два многоатомных элемента и влияние распространяется не через посредство одного из них, как в предыдущих примерах чрез посредство углерода, но двух, именно: углерода и кислорода пли, наоборот, чрез кислород и углерод. [12]
Страницы: 1