Кондуктометрическое определение
Cтраница 3
Для кондуктометрических определений используют реакции ком-плексообрйзования. [31]
Особенностью кондуктометрического определения рКа, отличающей его от соответствующего потенциометрического определения, является то обстоятельство, что серия экспериментальных данных в опыте получается при простом разбавлении, а не с помощью титрования раствором кислоты или щелочи постоянной концентрации. Поэтому кондуктометрический метод часто нуждается в поправках, связанных с активностью. Это делает весьма трудоемкими и без того громоздкие расчеты. [32]
Точность кондуктометрических определений снижается, если находящиеся в растворе примеси вступают в реакцию с определяемым веществом. В результате реакций нейтрализации, ком-плексообразования, окисления - восстановления и др. в растворе изменяются состав ионов и его электропроводность. Поэтому в каждом конкретном случае использования прямой кондуктометрии следует предусматривать возможность химических взаимодействий с посторонними веществами. [33]
Для кондуктометрического определения анионов широко применяется титрование нитратом серебра. Этот реагент дает возможность определять С1 -, Вг -, 1 -, SCN -, CrO - СзОТ, тартрат, цитрат и другие анионы. [34]
Для кондуктометрического определения анионов широко применяется титрование нитратом серебра. Этот реагент дает возможность определять СГ, ВГ, Г, SCNT, СгОГ, С2ОГ, тартрат, цитрат и другие анионы. [35]
Методы кондуктометрического определения тяжелых металлов основаны на изменении электропроводности растворов в момент прекращения связывания ионов [ Fe ( CN) e ] 4 - в труднорастворимое производное. Такое изменение устанавливается графически по кривой титрования и служит критерием точки эквивалентности. Если в процессе титрования последовательно изменяется состав образующегося осадка, то на кривой титрования появляется несколько изломов. [36]
Возможности кондуктометрического определения оснований различной силы и характер изменения электропроводности растворов при их титровании в общем аналогичны рассмотренным для кислот. Отличие заключается только в том, что при нейтрализации сильных оснований электропроводность понижается менее резко, чем при нейтрализации сильных кислот, так как подвижность ОН - ниже подвижности Н, и, наоборот, избыток титранта вызывает более резкое повышение электропроводности. Следует также заметить, что плавный ход кривых вблизи точек эквивалентности, наблюдаемый при титровании слабых оснований ( гидролиз образующихся солей), более заметен по сравнению с наблюдаемым для кислот такой же силы. Это объясняется тем, что при титровании - кислот в результате гидролиза в растворе - образуются гидр-оксильные ионы, а при титровании оснований - более подвижные водородные ионы. [38]
Возможность кондуктометрического определения солей слабых одноосновных кислот титрованием сильными кислотами, а также солей слабых одноосновных оснований титрованием сильными основаниями может быть установлена, если в качестве критериев использовать константы диссоциации слабых электролитов. Полнота реакции вытеснения слабого электролита зависит от концентрации соли. [39]
Критериями кондуктометрического определения солей слабых многоосновных кислот служат константы диссоциации кислот. [40]
При кондуктометрических определениях по методу осаждения искажение кривых титрования происходит вследствие некоторой растворимости осадка. В этих случаях полезно бывает в раствор добавлять этиловый спирт для понижения растворимости осадка. [41]
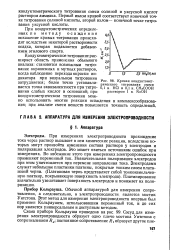 |
Кривая кондуктометрического титрования смеси 0 1 н. НС1 и 0 1 н. СНзСООН раствором 1 н NaOH. [42] |
При кондуктометрических определениях по методу осаждения искажение кривых титрования происходит вследствие некоторой растворимости осадка, которая подавляется добавлением этилового спирта. [43]
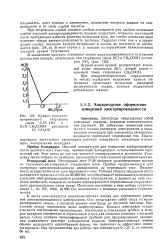 |
Кривая кондуктометрического титрования. [44] |
При кондуктометрических определениях по методу осаждения искажение кривых титрования происходит вследствие некоторой растворимости осадка, которая подавляется добавлением этанола. [45]
Страницы: 1 2 3 4