Фотометрическое определение - кобальт
Cтраница 2
Эти соединения имеют значение для фотометрического определения кобальта и его отделения от других элементов. Реакция протекает сложно, с образованием ряда промежуточных продуктов и побочными реакциями, что затрудняет исследование состава и свойств соединения. [16]
Другую группу органических реагентов, пригодных для фотометрического определения кобальта, составляют соединения с аминогруппами - амины и аминокислоты. Описаны методики определения кобальта с пиридиндикарбоновой, аминосалицило-вой, этилендиаминтетрауксусной и нитрилотриуксусной кислотами, а также с пиридином, этилендиамином, этилентриамином и трипиридилом. [17]
Монооксим 1 Г - динафтилдикетона применяется для фотометрического определения кобальта. [18]
Экстракция роданидов кобальта используется главным образом при фотометрическом определении кобальта в присутствии посторонних элементов ( см. стр. В некоторых случаях экстракционный метод применяется также для отделения кобальта перед определением другими методами или для очистки соединений кобальта. [19]
Хинолиндиоксим-5 8 применяется для обнаружения ряда элементов, фотометрического определения кобальта. [20]
Пршибил, Еник и Коброва [24] предлагают метод фотометрического определения кобальта дпэтилдитиокарба-матом натрия. В основу метода положено образование кобальтом зеленого соединения. [21]
Нитрозонафтол-2 [ 1 - 3, часто используемый для фотометрического определения кобальта, применяется и для экстракционного ( СНС13) отделения кобальта от других металлов перед его определением, например с помощью нитрозо - К-соли. [22]
Бис - ( 3-метиламинопропил) рубеановодородная кислота [866] применялась для фотометрического определения кобальта, причем раствор комплекса стабилизируют прибавлением гуммиарабика. Метод позволяет определить кобальт в присутствии никеля и меди. Измерение проводят ( в присутствии меди и никеля) при 430 ммк. [23]
ПАР и его комплексы более растворимы в воде; НАР применяется также для фотометрического определения кобальта, свинца и уранила [34] и других металлов. Для образующейся при рН3 протонированной формы ( HsR) характерна полоса поглощения при Х-395 нм; полоса довольно широкая, так что Н3К - форма ПАР заметно поглощает даже при 500 - 520 нм. Так же широка полоса молекулярной HjR-формы ПАР. При реакции со щелочами этот водород отщепляется только при рН 12 с образованием К2 - - формы. [24]
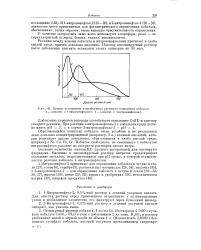 |
Кривые поглощения хлороформных растворов комплексов кобальта. 1 - комплекс с 1-нитрозонафтолом - 2. 2 - комплекс с 2-нитрозонафтолом - 1. [25] |
И 1-нитрозонафтол - 2 [25-28], и2 - нитрозонафтол-1 [28-33], одинаково часто применяемые для фотометрического определения кобальта, обеспечивают, таким образом, очень высокую чувствительность определения. [26]
Кроме отмеченных выше хелатообразующих реагентов, содержащих в качестве донорных атомов азот и кислород, для фотометрического определения кобальта можно также применять многочисленные серусо-держащие хелатообразующие реагенты, однако эти реагенты малоселективны. Следующие дитиолы - рубеановодородная кислота ( дитио-оксамид) ( I) [279, 985, 2402], N N - бuc - ( 3 - дuмeтuлaмuнonponuл) дuтuo - оксамид ( II) [986] и 2 3-хиноксалиндитиол ( III) [340] - образуют интенсивно окрашенные хелаты с Со, Си, Ni и менее интенсивно окрашенные с Fe, Mn и некоторыми платиновыми металлами. Эти элементы иногда можно определять без разделения, так как максимумы поглощения хелатов расположены при различных длинах волн ( стр. [27]
При соосаждении кобальта в присутствии Fe 3, A1, Cr 3, Sb 3, Ni, Си, Cd, Mn, Zn, Mg, Ba, Ca, T1 1, Na, Li в осадок соосадителя частично переходят Fe 3, Cu, Ni и следы хрома, влияние которых заметно сказывается на конечном фотометрическом определении кобальта. Для устранения захвата осадком соосадителя указанных элементов в исследуемый раствор перед введением реагентов вводят винную или щавелевую кислоты из расчета 2 - 3 г на конечный объем 100 мл. [28]
Для отделения мышьяка, сурьмьг меди, свинца, ртути, кадмия и других ионов от олива используют осаждение их в виде сульфидов в присутствии фторид-ионов, которые связывают олово. При фотометрическом определении кобальта в виде хлоридного или роданидного комплексов вредное влияние железа ( III) устраняют, связывая его в прочный фторидный комплекс. [29]
Методы отделения и фотометрического определения кобальта в виде соединении тетрароданида кобальта с крупными органическими катионами описаны на стр. Экстракция кобальта раствором трибутилфосфата из 10 N раствора соляной кислоты [407] позволяет выделить микрограммовые количества кобальта из металлического никеля. [30]
Страницы: 1 2 3