Зависимость - равновесная температура
Cтраница 1
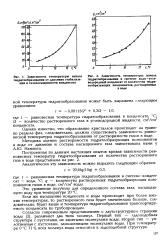
Зависимость равновесной температуры от входнойу0 для случая, когда в системе возможно несколько состояний равновесия, имеет гис-терезисный характер. Переход с участка кривой 05 на участок кривой DE осуществляется в точке бифуркации В при у Уо11 - При обратном движении, т.е. при уменьшении у0, мы будем двигаться сначала по участку. [1]
Ниже приводится зависимость равновесной температуры гидратообразования от давления для некоторых месторождений СССР. [2]
Для реальных растворов зависимость равновесной температуры от концентрации мономера в растворе имеет вид, показанный на рис. IV.3. Кривая 1 соответствует случаю отрицательного отклонения поведения раствора мономера от идеального, кривая 2 - положительного отклонения, кривая 3 - идеального раствора. [3]
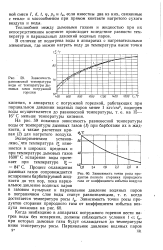 |
Зависимость равновесной температуры воды от температуры дымовых газов погружной горелки. [4] |
На рис. 59 показана зависимость равновесной температуры воды от температуры дымовых газов ( /) при барботаже их в жидкости, а также расчетная кривая ( 2) для нагретого воздуха. [5]
 |
Зависимость / Тр от концентрации мономера. / - отрицательное отклонение. 2 - положи. [6] |
На рис. II.1 представлена схематически зависимость равновесной температуры от логарифма концентрации мономера в растворе. [7]
На рис. IV-2 представлена схематически зависимость равновесной температуры от логарифма концентрации мономера в растворе. [8]
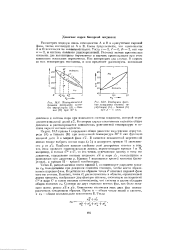 |
S. Ci. Иэитермичпсння фазоиан диаграмма системы сероуглерод ( А - бензил ( В jijw 30е С.| ИзоГшршш фазо-вал диаграмма системы сероуглерод ( Л - бензол ( В 1фтг р - - i атм. [9] |
Во втором случае постоянным является общее давление и рассматривается зависимость равновесной температуры и состава пара от со стаи а жидкости. [10]
Исследованы вопросы гидратообразования в конденсате Вуктыль-ского месторождения и показаны зависимости равновесной температуры образования гидратов от газонасыщенности воды и жидких углеводородов, даны графические и аналитические выражения этих зависимостей. [11]
На диаграммах температура - состав кривая пара Т ( Х2п) описывает зависимость равновесной температуры от состава пара при фиксированном давлении пара, а кривая жидкости Т ( Х2ж) описывает зависимость равновесной температуры системы от состава жидкой фазы при том же постоянном значении давления пара. В этом случае кривая пара проходит выше кривой жидкости. [12]
Криоскопические методы количественной оценки степени чистоты органических соединений основаны на термодинамическом анализе зависимости равновесной температуры процесса плавления или кристаллизации от доли закристаллизованного вещества. Когда имеют дело с малыми количествами исследуемого образца, эту зависимость определяют на основании кинетических кривых время - температура плавления, получаемых при линейном повышении температуры нагревательного блока. [13]
Однако известно, что образование кристаллов происходит на границе раздела фаз, следовательно, должна существовать зависимость равновесной температуры гидратообразования от растворимости газов в воде. [15]
Страницы: 1 2