Зависимость - теплота - испарение
Cтраница 2
В общем случае при интегрировании нужно учитывать зависимость теплот испарения или возгонки от температуры по уравнению Кирхгофа. [16]
При этом, конечно, затруднительно учесть зависимость теплоты испарения от температуры. [17]
Ур-ние ( 1) применяют для приближенного определения зависимости теплот испарения и сублимации от т-ры. Однако при точных вычислениях следует учитывать, что с изменением т-ры равновесное давление двухфазной системы изменяется. [18]
По этой диаграмме удобно определять тепловые эффекты процессов с учетом зависимости теплоты испарения смесей от их состава. [19]
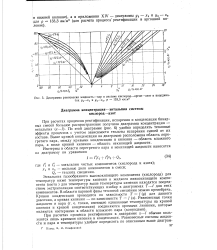 |
Диаграмма равновесия жидкость-пар в системе кислород-аргон-азот в координатах ( Ji-Xi и 1 / 2-хг, р 133 3. [20] |
По этой диаграмме ( рис. 6) удобно определять тепловые эффекты процессов с учетом зависимости теплоты испарения смесей от их состава. Выше кривой конденсации на диаграмме расположена область перегретого пара, между кривыми конденсации и кипения - область влажного пара, а ниже кривой кипения - область некипящей жидкости. [21]
Для определения давления р насыщенного пара вещества это уравнение следует проинтегрировать, что вполне осуществимо, если задана зависимость теплоты испарения от температуры. [22]
Уравнение ( 4), выражающее зависимость давления насыщенного пара от температуры ( приближенное из-за упрощений, введенных при интегрировании), можно уточнить, учтя зависимость теплоты испарения ( возгонки) от температуры. [23]
Уравнение ( 6), выражающее зависимость давления насыщенного пара от температуры ( приближенное из-за упрощений, введенных при интегрировании), можно уточнить, учтя зависимость теплоты испарения ( возгонки) от температуры. [24]
Теплоты испарения родственных соединений изменяются закономерно ( рис. IX. Это позволяет найти зависимость теплоты испарения от температуры для члена данного гомологического ряда, используя, например, принцип соответственных состояний и подобия свойств. [25]
О, HF и NH:) сдвинуты от линий в направлении, указывающем на некоторые дополнительные межмолекулярные взаимодействия, которые в других соединениях проявляются незначительно. На рис. 6.5 показана зависимость теплот испарения тех же веществ от положения элементов в периодической таблице. Из обоих графиков следует, что только гидриды F, О и N обладают значительным межмолекулярным взаимодействием, определяемым существованием сильных водородных связей, хотя и НС1 проявляет небольшие отклонения. [26]
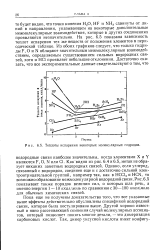 |
Теплоты испарения некоторых молекулярных гидридов. [27] |
HF и NH3 сдвинуты от линий в направлении, указывающем на некоторые дополнительные межмолекулярные взаимодействия, которые в других соединениях проявляются незначительно. На рис. 6.5 показана зависимость теплот испарения тех же веществ от положения элементов в периодической таблице. Из обоих графиков следует, что только гидриды F, О и N обладают значительным межмолекулярным взаимодействием, определяемым существованием сильных водородных связей, хотя и НС1 проявляет небольшие отклонения. [28]
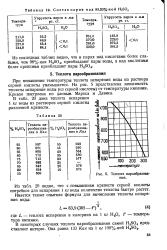 |
Состав паров над 99 23 % - ной H2S04.| Теплота парообразования. [29] |
При повышении температуры теплота испарения воды из раствора серной кислоты уменьшается. На рис. 5 представлена зависимость теплоты испарения воды ( из серной кислоты) от температуры кипения. Кривая построена по данным Маркса и Девиса. [30]
Страницы: 1 2 3