Зависимость - теплота - растворение
Cтраница 2
Для нас в этой главе особенно важна возможность дать количественное объяснение зависимости теплот растворения солей от концентрации в средах с невысокими значениями диэлектрической проницаемости с учетом ионной ассоциации в этих системах. Кроме того, открываются пути вычисления энергетических характеристик, которые могут послужить основой для проверки теорий сольватации и ассоциации ионов в средах с невысокими значениями диэлектрической проницаемости. [16]
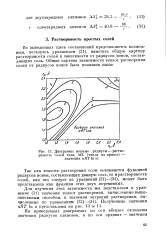 |
Диаграмма. ионные радиусы - растворимость солей типа MX ( числа на кривых - значения nRTlna. [17] |
Из выведенных здесь соотношений представляется возможным, пользуясь уравнением ( 31), наметить общую картину растворимости солей в зависимости от радиусов ионов, составляющих соль. Общая картина зависимости теплот растворения солей от радиусов ионов была показана выше. [18]
Галицкий [2] опубликовал результаты измерений теплот растворения KN03 и КаС03 в смешанном растворителе вода - этанол при постоянной концентрации солей ( т 0 9) и переменном содержании спирта от 0 до 28 мол. Им было замечено, что на изотерме зависимости теплоты растворения от состава смешанного растворителя в области около 15 мол. [19]
Галицкий [439] опубликовал результаты измерений теплот растворения KNO3 и К2СО3 в смешанном растворителе вода-этанол при постоянной концентрации солей ( т 0 9) и переменном содержании спирта от 0 до 28 % ( мол. Им было замечено, что на изотерме зависимости теплоты растворения от состава смешанного растворителя в области около 15 % ( мол. [20]
Галицкий [2] опубликовал результаты измерений теплот растворения KN03 и К2С03 в смешанном растворителе вода - этанол при постоянной концентрации солей ( т - - 0 9) и переменном содержании спирта от 0 до 28 мол. Им было замечено, что на изотерме зависимости теплоты растворения от состава смешанного растворителя в области около 15 мол. [21]
Интересны результаты исследования структуры водных растворов электролитов, выполненные в последние годы при помощи термохимических методов. Этот метод основан на измерении интегральных теплот растворения солей в воде и водных растворах кислот, при этом определяется зависимость теплот растворения соли от концентрации кислоты в растворителе. [22]
Интересны результаты исследования структуры водных растворов электролитов, выполненные в последние годы при помощи термохимических методов. Этот метод основан на измерении интегральных теплот растворения солей в воде и водных растворах кислот, при этом определяется зависимость теплот растворения соли от концентрации, кислоты в растворителе. [23]
Теплота растворения зависит от концентрации бутана. Кривая зависимости теплоты растворения от температуры, соответствующая постоянной концентрации, представляет собой плавную кривую, проходящую через критическую температуру для бутана. [24]
Теплота растворения зависит от концентрации бутана. Кривая зависимости теплоты растворения от температуры, соответствующая постоянной концентрации, представляет собой плавную кривую, проходящую через критическую температуру для бутана. [25]
Если же м умножают на уд. Эта величина обозначается через Q. Она тем более интересна, так как многие исследователи, например Ланг-берг, уже давно заметили зависимость теплоты растворения от сжатия и при этом ожидали, что эти величины можно определять одну из другой. [26]
Страницы: 1 2