Зависимость - интегральная теплота - растворение
Cтраница 1
Зависимость интегральной теплоты растворения от концентрации раствора неоднозначна: она может быть i, убывающей, экстремальной, постоянной. Например, ортофосфор-ная кислота растворяется в большом количестве воды экзотермично ( АДо - 13 4 кДж / моль), а в малом эн - 4 5 кДж / моль), что можно объяс-практически полным отсутствием диссоциации кислоты в крепких растворах. Интегральной теплотой раз-ошают тепловой эффект, сопровождаю-бесконечное разбавление раствора, содержащего вещества. [1]
Зависимость интегральной теплоты растворения от числа молей растворителя выражается графи - KCJM, эмпирическим уравнением или таблицей. [2]
Зависимость интегральной теплоты растворения от числа молей растворителя выражается графиком, эмпирическим уравнением или таблицей. [3]
Зависимость интегральных теплот растворения Nal, NaCl и КС1 в смешанном растворителе ( СНа) 4О3 - Н2О от содержания Af2 диоксана при т 0 05 и 25 С. [4]
Зависимость интегральных теплот растворения Nal, NaCl п КС1 при постоянных концентрациях солей т 0 05 от молярной доли диоксана N в смешанном растворителе диоксан - вода при 25 С. [5]
Сравнивая зависимости интегральных теплот растворения от состава, изображенные на рис. XI. [6]
Величину Qi вычисляют по зависимости интегральных теплот растворения от концентрации, используя справочные данные. [7]
В этих работах изучена зависимость интегральных теплот растворения от состава сополимеров и сделан вывод о степени уплотненности упаковки полимеров. [8]
На рис. 25 изображены зависимости интегральных теплот растворения КС1 в водных растворах MgS04, MgCl2 и LiCl переменной концентрации при различных температурах. [9]
В этих работах изучена зависимость интегральных теплот растворения от состава сополимеров и сделан вывод о степени уплотненности упаковки полимеров. [10]
На рис. 25 изображены зависимости интегральных теплот растворения КС1 в водных растворах MgS04, MgCl2 и LiCl переменной концентрации при различных температурах. [11]
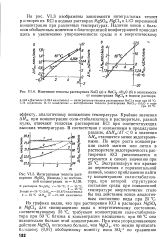 |
Изменение теплоты растворения NaCl ( а и МпС12 - 4Н2О ( б в зависимости.| Интегральные теплоты растворения MgSO4 ( безводн. до постоянной концентрации т 0 139. [12] |
На рис. VI.3 изображены зависимости интегральных теплот растворения К. [13]
Интегральную теплоту растворения определяют экспериментально, а дифференциальную вычисляют по зависимости интегральных теплот растворения от концентрации раствора. [14]
В случае полной диссоциации электролита, при наличии достаточно точных данных по зависимости интегральных теплот растворения от концентрации и концентрационной зависимости давлений насыщенных паров растворителя над растворами, AS может быть вычислена с вполне удовлетворительной точностью. В средах со средними и, особенно, низкими значениями диэлектрической проницаемости возникают затруднения, связанные с невозможностью одновременной надежной оценки степени диссоциации ( а) и активности. [15]
Страницы: 1 2