Зависимость - упругость - насыщенный пар
Cтраница 1
Зависимость упругости насыщенного пара от кривизны поверхности жидкости обусловливает целый ряд важных метеорологических явлений. Прежде всего следует подчеркнуть, что в свободной атмосфере нет тех плоских поверхностей, на которых мог бы конденсироваться водяной пар, насыщенный относительно плоской водной поверхности. Между тем возникновение облаков свидетельствует о том, что конденсация водяного пара в атмосфере происходит. Дело в том, что пар конденсируется на так называемых атмосферных ядрах конденсации: пылинках, частицах дыма, кристалликах морской соли и других мелких посторонних частицах, всегда взвешенных в воздухе в достаточном количестве. Адсорбируя молекулы водяного пара, эти ядра покрываются мономолекулярной пленкой воды, уподобляясь, таким образом, еодяпыя ттпелькам - достаточпо-крупногв-размера. [1]
Зависимость упругости насыщенного пара от кривизны поверхности жидкости обусловливает целый ряд важных метеорологических явлений. Прежде всего следует подчеркнуть, что в свободной атмосфере нет тех плоских поверхностей, на которых мог бы конденсироваться водяной пар, насыщенный относительно плоской водной поверхности. Между тем возникновение облаков свидетельствует о том, что конденсация водяного пара в атмосфере происходит. [2]
На рис. 82 представлена зависимость упругости насыщенного пара от температуры для воды. Для всех других веществ эта зависимость имеет такой же характер. [3]
Конденсационные манометрические термометры реализуют зависимость упругости насыщенных паров низкокипящей жидкости от температуры. Поскольку эти зависимости для используемых жидкостей ( хлористый метил, этиловый эфир, хлористый этил, ацетон и др.) нелинейны, следовательно, и шкалы термометров неравномерны. Однако, эти приборы обладают более высокой чувствительностью, чем газовые жидкостные. [4]
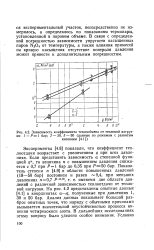 |
Зависимость коэффициента теплообмена от тепловой нагрузки. / - Р1 бар. 2 - 30, 3 - 50 ( данные по режимам с развитым. [5] |
В связи с определенной погрешностью зависимости упругости насыщенных паров N2O4 от температуры, а также влияния примесей на кривую насыщения отсутствие контроля давления может привести к дополнительным погрешностям. [6]
Кистяковский, Голицын и Шиллер исследовали зависимость упругости насыщенного пара от формы поверхности жидкости и внешних сил, действующих на эту поверхность. Ими были выведены основные соотношения, устанавливающие изучаемую зависимость, которые в 1870 г. - в первичном виде были даны Томсоном, Шиллер показал, что испарение жидкости ускоряется при увеличении давления газа на ее поверхность. [7]
Формула Клапейрона ( 76) описывает зависимость упругости насыщенных паров от температуры. Например, для вольфрама А 12 24; В 4 026 - 10 - 2, если давление выражено в торах. [8]
Метод Улиха также хорошо применим к вычислению зависимости упругости насыщенного пара жидкостей от температуры. [9]
Чаще всего для определения скрытой теплоты парообразования используется зависимость упругости насыщенного пара от температуры. [10]
Истинные химические константы J вычисляются на основании экспериментальных данных по зависимости упругости насыщенного пара от температуры или теоретическим путем с помощью методов статистической физики. Их также можно вычислить из условий равновесия, если экспериментально определены константы равновесия К, реакций. [11]
Теплота испарения и сублимации нитроформа была рассчитана на основе экспериментального определения зависимости упругости насыщенного пара над жидким и твердым тринитрометаном в интервале температур от 7 до 44 С. [12]
Ряд полученных значений упругости пара и соответствующие им температуры дают возможность найти уравнение зависимости упругости насыщенного пара от температуры для данной жидкости. [13]
Карно, проводимый со смесью жидкости и насыщенного пара над ней в качестве рабочего вещества, можно установить связь между зависимостью упругости насыщенных паров от температуры и теплотой парообразования. Однако все приведенные там рассуждения остаются в силе и тогда, когда в качестве рабочего вещества берется смесь твердой и жидкой фаз какого-либо тела. [14]
Анализ этого уравнения позволил Михаилу Степановичу предсказать все возможные случаи изменения состава пара с температурой, обосновать количественно наблюденные особенности водно-спиртовых растворов и, в частности, дать исчерпывающую характеристику зависимости состава пара азеотропа от температуры для случаев максимума и минимума на кривой, выражающей зависимость упругости насыщенного пара от концентрации. [15]
Страницы: 1 2