Низшая орбита
Cтраница 1
Низшие орбиты tyl и г 52 в основном состоянии бутадиена заняты четырьмя электронами. Переход с г до г з2 в этилене сильно уменьшает длину волны электрона и поэтому требует значительной энергии. Поскольку переход в бутадиене не уменьшает в такой же степени длину волны электрона, бутадиен поглощает при больших длинах волн ( меньшая энергия возбуждения), чем этилен. Идея в основном сводится к свободноэлектронной модели сопряженных систем. Метод с соответствующими уточнениями дает хорошие результаты при количественных расчетах спектров сопряженных систем. [1]
Низшие орбиты tyl и г) в основном состоянии бутадиена заняты четырьмя электронами. Переход с г), до г) 2 в этилене сильно уменьшает длину волны электрона и поэтому требует значительной энергии. Поскольку переход IJV B бутадиене не уменьшает в такой же степени длину волны электрона, бутадиен поглощает при больших длинах волн ( меньшая энергия возбуждения), чем этилен. Идея в основном сводится к свободноэлектронной модели сопряженных систем. Метод с соответствующими уточнениями дает хорошие результаты при количественных расчетах спектров сопряженных систем. [2]
При переводе я л электрон перемещается с низшей орбиты на высшую. [3]
При переводе л - п электрон перемещается с низшей орбиты на высшую. [4]
С помощью этого последнего способа можно рассчитывать и такие возбужденные состояния, при которых, например, один электрон перешел с низшей орбиты на высшую. [5]
МО будут для ясности пронумерованы в порядке возрастания энергии, как указано на рис. 1 - 8; из них четыре низших орбиты являются занятыми. [6]
Поэтому К и л основного состояния нечетного ядра совпадают с И и л орбиты нечетного нуклона. Все низшие орбиты нейтронов и протонов попарно заполнены. [7]
Принцип запрета Паули делает понятной оболочечную структуру атома. Если все состояния на низших орбитах уже заполнены электронами, то новой частице не остается ничего другого, как занять свободное место на более высокой орбите. Более того, этот принцип позволяет понять правило Рид-берга для числа электронов в заполненной оболочке атома. [8]
Надо было делать специальное предположение, - на низших орбитах атома может находиться лишь ограниченное число электронов. [9]
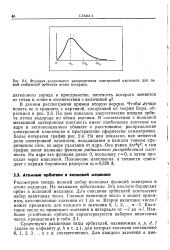 |
Функция радиального распределения электронной плотности для самой стабильной орбитами атома водорода. [10] |
Чтобъ Лучше понять ее и сравнить с картиной, следующей из теории Бора, обратимся к рис. 2.3. На нем показана энергетически низшая орбита атома водорода по обеим версиям. В соответствии с волновой механикой электронная плотность имеет наибольшее значение на ядре и экспоненциально убывает с расстоянием; распределение электронной плостности в пространстве сферически симметрично. Более интересен график рис. 2.4. На нем показано, как меняется доля электронной плотности, находящаяся в каждом тонком сферическом слое, по мере удаления от ядра. Она равна 4яг2о А а сам график носит название функции радиального распределения плот ности. На ядре эта функция равна 0, поскольку г0, а затем проходит через максимум. Положение максимума в точности совпадает с первым боровским радиусом а00 529 А. [11]
Паули была установлена закономерность, согласно которой в одном квантовом состоянии может находиться не более одного электрона. Вследствие принципа Паули в многоэлектронном атоме все электроны не могут находиться на низшей орбите и распределение их по орбитам в невозбужденном состоянии является строго определенным. [12]
Страницы: 1