Орбиталь
Cтраница 1
Орбиталь п симметрична, а п - антисимметрична относительно поворота вокруг оси С-2 - элемента симметрии, который сохраняется в любой конформашш молекулы гидразина. [1]
 |
Образование и структура sp - гибридных орбиталей. [2] |
Орбиталь имеет только положительный знак, а р-орбиталь имеет положительную и отрицательную части. Положительная часть комбинируется cs - орбиталью, а отрицательная уменьшается вследствие слияния. [3]
Орбиталь соответствует одинарной, простой химической связи; электроны, локализованные на этой орбитали, называются о-электронами. Они обычно являются сильно связывающими, электронами и в значительной мере локализованы. Орбиталь соответствует одной из связей в атомной группе с кратной связью. Каждой о - и я-орбиталям соответствуют разрыхляющие ( свободные в основном состоянии) о и я - орбитали. [4]
Орбиталь соответствует ординарной, простой химической связи; электроны, локализованные на этой орбитали, называются ог-электронами. Они обычно являются сильно связывающими электронами и в значительной мере локализованы. Орбиталь соответствует одной из связей в атомной группе с кратной связью. Каждой а - и я-орбиталям соответствуют разрыхляющие ( свободные в основном состоянии) о - и л - орбитали. [5]
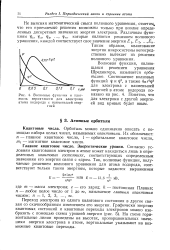 |
Волновые функпии и плотность вероятности для электрона атома водорода с наименьшей энергией. [6] |
Орбиталь можно однозначно описать с помощью набора целых чисел, называемых квантовыми. Их обозначают: п - главное квантовое число, / - орбитальное квантовое число, mi - магнитное квантовое число. [7]
Орбиталь представляет собой почти неподеленную пару электронов, сконцентрированную, как показывает расчет, на атоме углерода, но вне связи С - О. Имея высокую концентрацию электронного заряда, эти орбитали создают отрицательный полюс диполя на атоме углерода. Следует заметить, что в рассмотренных выше молекулах галогеноводородов неподеленные пары на атомах галогена вносят решающий вклад в отрицательную полярность атомов галогена в этих молекулах. [8]
Орбиталь с еще большей энергией имеет две узловые плоскости. [9]
Орбиталь а симметрична относительно отражения в этой плоскости, а 02 и 03 несимметричны. Дальнейшая дело-кализация состоит в том, чтобы примешать 0J и 02 - 0з в 02 - 0з и 02 0з в симметричные комбинации. Это эффект второго порядка, однако он может иметь значение для химии. [10]
Орбиталь менее устойчива, чем 2pz, и она имеет заметно выраженный 2р2 - характер. [11]
Орбиталь ф1о представляет собой почти чистую ls - АО кислорода. [12]
Орбиталь является правильной волновой функцией для атома водорода, будучи собственной функцией операторов Н, М2 и Mz; а 2рх - и 2р - орбитали - собственные функции Н и М2, но не Mz. Однако при переходе к рассмотрению свойств, зависящих от каких-либо компонент углового момента, необходимо использовать только правильные орбитали. [13]
Орбиталь dZ2 имеет другую форму: ее лопасти ориентированы вдоль оси z, а кольцо окружает ось z и имеет максимум в плоскости ху. [14]
 |
Возможные комбинации 1s - орбитали водорода и 2р - орбиталей фтора ( перекрывание показано горизонтальной штриховкой. [15] |
Страницы: 1 2 3 4 5