Орбиталь - бериллий
Cтраница 1
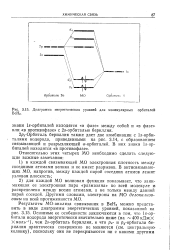 |
Диаграмма энергетических уровней для молекулярных орбиталей ВеН2. [1] |
Орбиталь бериллия также дает две комбинации с ls - орби-талями водорода, приведенными на рис. 3.14, с образованием связывающей и разрыхляющей оорбиталей. [2]
 |
Образование гибридных орбиталей при смешивании 2л и 2 / 7г - орбиталей. [3] |
Орбиталь бериллия имеет одну и ту же амплитуду в любом направлении. [4]
 |
Схема перекрывания р - АО фтора и s -, р - и гибридной q ( sp - AO бериллия. Одна гибридная орбиталь бериллия для наглядности показана смещенной вверх от общей оси. [5] |
Перекрывание гибридных sp - орбиталей ато-ма бериллия с р - АО атомов фтора также изображено на рис. 4.27. Благодаря вытянутой форме гибридных орбиталей достигается более полное перекрывание электронных облаков, в итоге образуются более прочные химические связи. Энергия, выделяющаяся при образовании этих связей, больше, чем суммарные затраты энергии на возбуждение атома бериллия и гибридизацию его атомных орбита-лей. Поэтому процесс образования молекулы BeF-2 энергетически выгоден. [6]
 |
Линейная молекула ВеС1. [7] |
Связи, образовавшиеся за счет перекрывания двух sp - орбиталей бериллия с р-орбиталями атомов хлора, показаны на рис. 5.10. Атомы расположены линейно; такое же расположение атомов предсказывает и теория Сиджвика - Пауэлла. [8]
 |
Энергетическая диаграмма P6 TaJIf линейной трехатомной мо-лекулы без тг-связывания на примере ВеНо. [9] |
В соответствии с большей электроотрицательностью водорода его орбитали в схеме расположены ниже орбиталей бериллия. [10]
 |
Форма и расположение sp - гибрйДных электронных облаков. [11] |
Таким образом, в молекуле ВеС12 оба атома хлора присоединяются одинаковыми sp - гибрядными орбиталями бериллия. Экспериментальные данные показывают, что молекулы галогенидов Be, Zn, Cd, Hg линейны и в них обе связи имеют одинаковую длину. [12]
Это описание формально - в действительности у атома бериллия нет пустых гибридных орбита-лей, но те связи, которые возникают при образовании иона [ ВеСЦ ] 2 -, можно описать как состоящие из Зр-орбиталей хлора и свободных ( вакантных) р3 - орбиталей бериллия. [13]
Такая цепочка представляет собой конечный результат комбинации двух связей: одна, нормальная, связь возникает, потому что электрон от хлора вместе с электроном от бериллия образуют электронную пару, а вторая - потому что атом хлора передает свою электронную пару на пустую валентную орбиталь бериллия. [15]
Страницы: 1 2
