Зависимость - энтальпии
Cтраница 1
Зависимость энтальпии ( внутренней энергии) от температуры для равновесной смеси проходит выше соответствующей зависимости для продуктов завершенной реакции ( рис. 50), так как тепловой эффект незавершенной реакции ДЯ2 меньше, чем завершенной ДЯ3 при одинаковой конечной температуре. Степень завершенности реакции зависит от условий протекания реакции и определяется величиной константы равновесия, которая устанавливает соотношение между веществами в равновесной смеси. Связь между степенью завершенности реакции ( Д, х, а) и константой равновесия / С была получена выше. Из сказанного следует, что выражение для теплового эффекта реакции должно учитывать степень завершенности реакции. [1]
 |
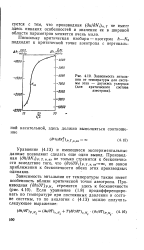
К определению равновесной температуры сгорания при наличии диссоциации продуктов полного сгорания. [2] |
Зависимость энтальпии ( внутренней энергии) от температуры для равновесной смеси, включающей продукты диссоциации, проходит круче соответствующей зависимости для продуктов полного сгорания, так как процессы диссоциации связаны с поглощением теплоты. Эта зависимость показана на рис. 52 пунктирной линией. При стандартной температуре ( Т 298 К) обе кривые практически совпадают. [3]
 |
Зависимость энтальпии от температуры для системы этан - двуокись углерода ( для критического состава азеотропа. [4] |
Зависимость энтальпии от температуры также имеет особенность вблизи критической точки азеотропа. [5]
 |
Поликонцентрата - изотерма химического потенциала. [6] |
Зависимость энтальпии от температуры реализуется через тепло - - емкость. Теплоемкость С - количество теплоты 6Q ( Дж), необходимой для изменения температуры единицы массы или количества вещества ( кг, кмоль) на 1 К. [7]
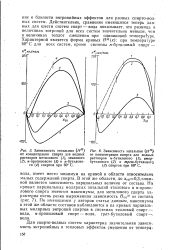 |
Зависимость энтальпии ( Н от концентрации спирта для водных растворов н-бутилового ( /, втор-бутилового ( 2 и / п /. е / и-бутиловогз ( 3 спиртов при 60 С. [8] |
Зависимость энтальпии ( Нм) от концентрации спирта для водных растворов метилового ( 1), этилового ( 2), и-пропилового ( 3) и н-бутилово-го ( 4) спиртов при 60 С. [9]
Зависимость энтальпии жидкости и пара от давления ( при умеренных давлениях) незначительна и обычно в технических расчетах не учитывается. [11]
Зависимость энтальпии реального газа от давления хорошо видна и на рис. 1 - 31, где в координатах г, t представлены изобары для водяного пара. [12]
Зависимость энтальпии твердого тела от давления настолько мала, что изменением энтальпии твердого тела при изменении внешнего давления, действующего на это твердое тело, практически можно пренебречь. [13]
Зависимость энтальпии реальных газов от давления согласно приближенному обобщенному методу расчета приведена на фиг. [14]
Зависимость энтальпии чистого компонента от давления и температуры изображается обычно в виде диаграмм. [15]
Страницы: 1 2 3 4 5
