Зависимость - тепловой эффект - реакция
Cтраница 1
Зависимость тепловых эффектов реакции от температуры ( закон Кирхгофа) обусловливается зависимостью от температуры теплоемко-стей веществ участвующих в реакции. [1]
Зависимость тепловых эффектов реакции от температуры обусловливается изменениями теплоемкости системы от температуры. [2]
Зависимость теплового эффекта реакции от температуры определяется разностью теплоемкостей исходных веществ и продуктов реакции. [3]
Зависимость тепловых эффектов реакции от температуры ( закон Кирхгофа) обусловливается зависимостью от температуры теплоемко-стей веществ участвующих в реакции. [4]
Составить уравнение зависимости теплового эффекта реакции С ( графит) Н2О СО Н2 от температуры. [5]
Рассмотрим теперь вопрос о зависимости тепловых эффектов реакции от параметров, характеризующих состояние системы. [6]
Это положение, устанавливающее зависимость теплового эффекта реакции от температуры, называется законом Кирхгофа. [7]
Другая важная термохимическая закономерность - зависимость теплового эффекта реакции от температуры, выраженная формулой Кирхгофа. [8]
Первое начало термодинамики позволяет определить зависимость теплового эффекта реакции от температуры. Представим себе следующий круговой процесс. [9]
 |
Зависимость теплового эффекта химической реакции от температуры. [10] |
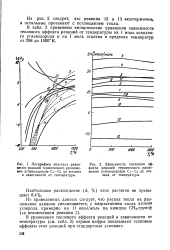
Кривые на рис. 1.2 выражают зависимость теплового эффекта реакции от температуры. [11]
Другой важной термохимической закономерностью является зависимость теплового эффекта реакции от температуры, выражаемая формулой Кирхгоффа. [12]
Первое начало термодинамики позволяет определить зависимость теплового эффекта реакции от температуры. Представим себе следующий круговой процесс. Пусть реакция протекает при температуре То, причем выделяется количество теплоты Qo. Затем продукты реакции нагреваются до температуры Т, на что нужно затратить количество теплоты, равное С ( Т - Т0), где Ci-сумма мольных теплоемкостей продуктов реакции, умноженных на коэффициенты при формулах этих веществ в уравнении реакции. Если при этой новой температуре направить реакцию в обратную сторону, то получатся снова первоначальные вещества. [13]
В табл. 2 приведены эмпирические уравнения зависимости теплового эффекта реакций от температуры на 1 моль исходного углеводорода и на 1 моль этилена в пределах температур от 298 до 1500 К. [15]
Страницы: 1 2