Зависимость - гидролиз
Cтраница 1
Зависимость гидролиза от температуры иллюстрируется двумя следующими опытами. [1]
Зависимость гидролиза амида - ацетил - Ь - фенилаланил - Ь - тирозина, катализируемого пепсином. [2]
Зависимость гидролиза амида М - ацетил - Ь - фенилаланил - Ь - тирозина, катализируемого пепсином. [3]
Зависимости гидролиза олнгосахаридных модельных субстратов лизоцима, с одной стороны, и бактериальной клеточной стенки, с другой, являются различными. В отличие от этого константа скорости бактериолитического действия лизоцима контролируется ионогенными группами с рК 5 0 и 9 2, первая из которых является каталитической и участвует в реакции в анионной форме. Вторая группа, как показано при изучении конфор-мационной стабильности лизоцима под действием ультразвука, в паре с противоположно заряженной ионогенной группой, имеющей аномально низкое значение рК ( ниже 2 0), может образовывать солевой мостик, поддерживая каталитически активную конформацию активного центра фермента. В кинетике ферментативного лизиса клеточной стенки проявляется только группа с рК 5 0 ( по-видимому, карбоксилат-ион Asp 52), функция которого может заключаться в стабилизации образующегося в каталитической реакции карбокатиоиа. [4]
Полученные нами данные о зависимости гидролиза от углеводного компонента находятся в хорошем соответствии с современными представлениями о механизме кислотного гидролиза и о конформа-циях Сахаров [17] и, в свою очередь, являются новым материалом, подтверждающим эти представления. [5]
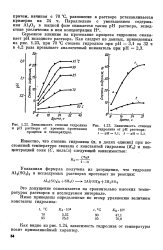 |
Зависимость степени гидролиза. [6] |
Как видно из рис. 1.24, зависимость гидролиза от температуры носит прямолинейный характер. [7]
Эта работа ясно продемонстрировала качественный характер зависимости гидролиза от микротактичности. Ограничение в применении метода к полимерам с реакционноспособными заместителями также не может быть преодолено. Однако при дальнейшем развитии методики возможно открытие реакций, более специфичных к распределению диастереопоследовательностей. [8]
В самых последних работах [586] также обстоятельно изучен процесс гидролиза уранил-иона, исследована зависимость гидролиза от температуры и ионной силы раствора. [9]
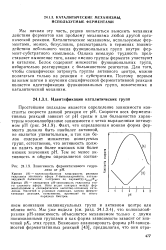 |
Зависимость ферментативного гидро -. лиза от рН.. [10] |
Кривая ( А) - колоколообразная зависимость реакции гидролиза этилового эфира Л - бензоиларгинина, катализируемой папаииом; построена по параметру KK j Кривая ( В) - ожидаемая рН - зависимость гидролиза этого сложного эфира. Ясно виден контраст между ферментативным и специфическим кислотно-основным катализом. Масштаб в условных единицах, однако ферментативная реакция, естественно, протекает на много порядков быстрее. [11]
Во всяком случае, физический смысл этого предположения достаточно ясен. Более того, в случае лизоцима, например, рН - зависимости гидролиза различных олигосахаридов действительно различаются, что не противоречит высказанной здесь гипотезе. [12]
Влияние рН на ферментативную активность иногда можно объяснить в рамках модели, предполагающей, что катализ зависит от состояния ионизации некоторых аминокислот. Тогда, если зависимость & кат / Лм от рН описывается колоколообразной кривой, по ней можно определить константы ионизации К е и Kze каталитически важных групп в свободном ферменте. Однако имеющиеся данные довольно скудны. Кривые зависимости АкатА / См от рН оказались колоколообразными, что предполагает участие в катализе как кислой, так и основной групп. Отсутствие данных, указывающих на титрование второй группы в комплексе ES, не исключает возможности участия в реакции кислотного катализа, если предположить, например, что соответствующая стадия не лимитирует скорость реакции ( ср. Зависимость гидролиза КГФ от рН представлена в нескольких ранних работах. По зависимости начальной скорости от рН [104] были определены величины P / CES равные 6 5 и 8 6, однако сравнение с ацилтрипептидами показывает, что эти данные нуждаются в уточнении. [13]
Страницы: 1