Бихромат - натрий
Cтраница 1
Бихромат натрия отсутствует в значительных дозах в природной воде, но хорошо в ней растворяется. Он относительно дешев, а малые его концентрации сравнительно легко определяются колориметрическим методом. Хлорид натрия очень дешев и доступен, а сопротивление его раствора пропорционально концентрации в широком диапазоне, но он присутствует в природной воде и неприменим при очень слабых концентрациях. Рода-мины отсутствуют в природной воде и допускают определение при очень малых концентрациях Сх min, но они не очень хорошо растворяются и дорогостоящие. Чаще всего применяют хлорид натрия, но если измеряемая вода сама содержит его в заметном количестве, то во избежание очень большого расхода хлорида натрия переходят на другой индикатор, в частности на бихромат натрия. Учитывая токсичность последнего, его окончательная концентрация Сх должна быть во много раз меньше, чем хлорида натрия. [1]
Бихромат натрия Na2Cr2O7 производят не только для выделения Сг2О3 и получения из него металлического хрома. [2]
Бихромат натрия технический ( хромпик натриевый) Na2Cr207 nH20 - натриевая соль двухромовой кислоты. [3]
Бихромат натрия или калия в растворе, подкисленном серной кислотой, широко используется для окисления первичных и вторичных спиртов. В результате окисления первичные спирты превращаются в альдегиды, вторичные - в кетоны. Чтобы предотвратить превращение альдегидов во время синтеза в кислоты, необходимо удалять альдегиды по мере образования из сферы реакции. При действии на первичные спирты избыточного количества бихромата и серной кислоты, наряду с кислотами, образуются и сложные эфиры. Это объясняется этерификацией исходного спирта кислотой, образующейся при его окислении. [4]
Бихромат натрия или калия в растворе, подкисленном серной кис-логой, широко используется для окисления первичных и вторичных спиртов. В результате окисления первичные спирты превращаются в альдегиды, вторичные - в кетоны. [5]
Бихромат натрия является исходным продуктом для получения многих хромовых соединений. [6]
Бихромат натрия Na2Cr2O7 производят не только для выделения Сг2О3 и получения из него металлического хрома. [7]
Бихромат натрия Na2Cr207 - 2H20 в больших количествах применяют при выделке кожи ( при производстве так называемой. Хром с белком, присутствующим в коже, образует нерастворимое соединение. [8]
Бихромат натрия технический ( хромпик натриевый) NasC Oj пН20 - натриевая соль двухромовой кислоты. [9]
Бихромат натрия добавляется в исходный раствор для того, чтобы перевести четырехвалентный плутоний в шестивалентный, соединения которого лучше всего экстрагируются гексоном; кроме того, четырехвалентный плутоний при низкой кислотности легко гидролизуется с образованием неэкстрагируемых полимерных соединений. Во второй колонне органическая фаза, содержащая нитраты уранила и плутонила, подвергается реэкстрак ции водным раствором нитрата алюминия, содержащим восстановитель. Последний, восстанавливая плутоний до трехвалентного, переводит его в водную фазу, в то время как высаливающий агент удерживает уран в органической фазе. Уран извлекается из этой фазы разбавленной азотной кислотой в третьей колонне. [10]
Бихромат натрия ( двухромовокислый натрий) NaaCr2O7 - 2H2O ( мол. [11]
Бихромат натрия получается окислением хромистого железняка FeO - Cr2O3 кислородом воздуха, в присутствии соды, при высокой температуре. [12]
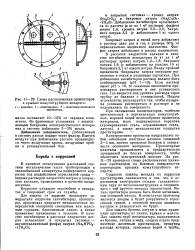 |
Схема расположения протекторов в крышке кожухотрубного аппарата. [13] |
Бихромат натрия и едкий натр добавляют в раствор один раз в год в размере 50 % от первоначально введенного количества. Фосфат натрия добавляют в рассол ежемесячно. [14]
Бихромат натрия или калия в растворе, подкисленном серной кислотой, широко используется для окисления первичных и вторичных спиртов. В результате окисления первичные спирты превращаются в альдегиды, вторичные - в кетоны. Чтобы предотвратить превращение альдегидов во время синтеза в кислоты, необходимо удалять альдегиды по мере образования из сферы реакции. При действии на первичные спирты избыточного количества бихромата и серной кислоты, наряду с кислотами, образуются и сложные Эфиры. Это объясняется этерификацией исходного спирта кислотой образующейся при его окислении. [15]
Страницы: 1 2 3 4