Бициклогептадиен
Cтраница 1
Двойные связи бициклогептадиена являются реакционноспособными. [1]
 |
Селективное гидрирование изомерных гексадиенов ( 0 2 М, катализируемое. [2] |
Интересно, что бициклогептадиен, в котором две двойные связи не могут вступить в сопряжение, подвергается скелетной перегруппировке и в результате в качестве конечного продукта вместо бицикло-гептена образуется этилиденциклопентан. [3]
Это соединение получают окислением органическими надкис-лотами соответствующего бициклогептадиена, полученного отщеплением НС1 щелочью ( спиртовым раствором) от аддукта гек-сахлорциклопентадиена и хлористого винила. [4]
Уинстейн [123] сообщил о токсичности продуктов бромирования бициклогептадиена, работа с которыми имела трагические последствия. По-видимому, токсичные алкилгалогениды должны занимать промежуточное положение между алкилгалогенидами, которые гидролизуются слишком медленно ( и потому оказываются безвредными), и теми, которые гидролизуются настолько быстро, что разрушаются до того, как попадут в организм. [5]
СО) 2 [ Р ( СбН5) з ] 2 в реакции присоединения ацетилена к бициклогептадиену, который по свойствам близок к сопряженным диенам ( S с h r a u s е г G. [6]
Особенный интерес для полимеризации в качестве исходных мономеров представляют 3-метилбутен - 1 и циклические мономеры - винилцик-логексен, бициклогептадиен, которые дают термостойкие полимеры. Метилбутен-1 содержится в пентан-амиленовой фракции крекинг-бензина, однако удобных способов его выделения еще не найдено. [7]
Кольцевая система квадрициклена является высоконапряженной, и при перегонке при нормальном давлении ( около 100 С) этот углеводород медленно превращается в исходный бициклогептадиен. Следует обратить внимание на то, что соединения I и II, а также III и IV представляют собой валентные изомеры; поскольку же обе пары соединений способны к взаимопревращению, они являются таутомерами. [8]
В стеклянную ампулу помещают 7 4 г ( 0 028 г-моля) 5-этилпен-тахлорциклопентадиена и 6 5 г ( 0 07 г-моля) бициклогептадиена. Ампулу нагревают на масляной бане до температуры 135 - 140 и выдерживают 20 час. После охлаждения ампулу вскрывают, избыток бициклогептадиена отгоняют на водяной бане, а остаток фракционируют в высоком вакууме. [9]
Так как в соответствии с правилом Бредта в мостиковых системах двойная связь не может находиться при узловом атоме, перемещение двойных связей в бициклогептадиене невозможно. По этой причине последний не способен превращаться в сопряженный изомер; сходное положение имеет место и в случае дициклопентадиена. Эти два диолефина являются ценным сырьем для получения диальдегидов методом оксосинтеза [51], так как другие диолефины в условиях этого процесса превращаются в более термодинамически устойчивые сопряженные изомеры, а сопряженная двойная связь в условиях оксопроцесса подвергается гидрированию, но не гидроформилирова-нию. [10]
С другой стороны, толуол получается из циклогепта-триена-1 3 5 в основном состоянии, и, поскольку влияние давления: на состояния, из которых образуются бициклогептадиен и толуол, различно, мы приходим к выводу, что это разные состояния. Отсюда однозначно следует, что толуол получается через состояние S, поскольку с самого начала мы предположили, что триплеты в реакции не участвуют. [11]
 |
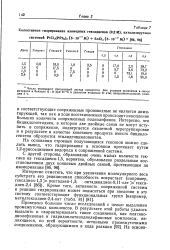
Спектр ЯМР высокого разрешения бицикло - - гентадиена. [12] |
Сравнение спектров ЯМР продукта и исходного вещества позволяет установить строение первого. Бициклогептадиен имеет три группы протонных резо-нансов при - 368, - 173 и - 81 гц ( 60 мггц), считая от поглощения тетра-метилсилана ( внутренний стандарт), в области слабого поля. [13]
Квантовый выход образования толуола при р О, полученный экстраполяцией зависимости 1 / фТОлуол от давления циклогептатриена-1 3 5 ( по уравнению Штерна-Фольмера), близок к единице. Напротив, выход бициклогептадиена слабо зависит от давления, и соединение XXV образуется и в растворе. [14]
В стеклянную ампулу помещают 7 4 г ( 0 028 г-моля) 5-этилпен-тахлорциклопентадиена и 6 5 г ( 0 07 г-моля) бициклогептадиена. Ампулу нагревают на масляной бане до температуры 135 - 140 и выдерживают 20 час. После охлаждения ампулу вскрывают, избыток бициклогептадиена отгоняют на водяной бане, а остаток фракционируют в высоком вакууме. [15]
Страницы: 1 2