Кривая зависимость - плотность - ток
Cтраница 1
Кривые зависимости плотности тока на катоде от напряжения являются важной характеристикой электродного процесса. Эта зависимость определяется природой металла, составом электролита, материалом и состоянием поверхности катода, а также соотношением анодных и катодных поверхностей, их взаимным расположением и объемной плотностью тока. Поскольку эти параметры могут сильно изменяться в каждом конкретном случае, то приведенные в таблицах расчетные величины нельзя рассматривать как абсолютно точные. [1]
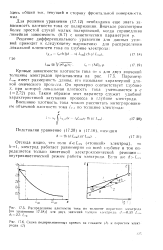
Кривые зависимости плотности тока от х для двух значений толщины электродов представлены на рис. 17.5. Параметр Law имеет размерность длины; его называют характерной длимой омического процесса. Он примерно соответствует глубине - V, при которой локальная плотность тока уменьшается в в ( - 2 72) раз. Таким образом этот параметр служит удобной характеристикой затухания процесса в глубине электрода. [3]
Поэтому при определенных допущениях построение изопотенциальных кривых зависимости плотности тока от обратной температуры позволяет рассчитать по углу наклона полученных прямых эффективную энергию активации. Значение энергии активации порядка 13 - 21 кДж / ыоль ( 3 - 5 ккал / моль) свидетельствует о диффузионных затруднениях в процессе, а порядка 38 - 50 кДж / моль ( 9 - 12 ккал / моль) и выше - о кинетических. [4]
Поэтому при определенных допущениях построение изопотенциальных кривых зависимости плотности тока, от обратной температуры позволяет рассчитать по углу наклона полученных прямых эффективную энергию активации. Значение энергии активации порядка 13 - 21 кДж / моль ( 3 - 5 ккал / моль) свидетельствует о диффузионных затруднениях в процессе, а порядка 38 - 50 кДж / моль ( 9 - 12 ккал / моль) и выше - о кинетических. [5]
 |
Перенапряжение выделения водорода на различных металлах. [6] |
При этом результаты измерений обычно представляют в виде поляризационных кривых - кривых зависимости плотности тока на электроде от величины поляризации. Вид поляризационной кривой того или иного электродного процесса отражает особенности его протекания. Методом поляризационных кривых изучают кинетику и механизм окислительно-восстановительных реакций, работу гальванических элементов, явления коррозии И пассивности металлов, различные случаи электролиза. [7]
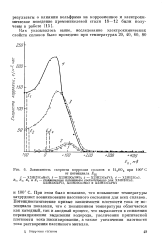 |
Зависимость скорости коррозии сплавов в H2S04 при 100 С. [8] |
При этом было показано, что повышение температуры затрудняет возникновение пассивного состояния для всех сплавов. Потенциостатические кривые зависимости плотности тока от потенциала показали, что с повышением температуры облегчается как катодный, так и анодный процесс, что выражается в снижении перенапряжения выделения водорода, увеличении критической плотности тока пассивирования, а также увеличении плотности тока растворения пассивного металла. [9]
На рис. 1 - 2 приведены значения плотности тока при поляризации в хлоридных растворах с потенциалом около 1 9 В для образцов гитана с поверхностью различной обработки. Одинаковые формы кривых зависимости плотности тока от потенциала на Pt и Ti позволяют предположить, что на обеих поверхностях электрода происходят одинаковые анодные процессы. [10]
На рис. 1 - 2 приведены значения плотности тока при поляризации в хлоридных растворах с потенциалом около 1 9 В для образцов титана с поверхностью различной обработки. Одинаковые формы кривых зависимости плотности тока от потенциала на Pt и Ti позволяют предположить, что на обеих поверхностях электрода происходят одинаковые анодные процессы. [11]
 |
Перенапряжение выделения водорода на различных металлах. [12] |
Выяснение связи между величиной поляризации и скоростью электродного процесса является важнейшим методом изучения электрохимических процессов. При этом результаты измерений обычно представляют в виде поляризационных кривых - кривых зависимости плотности тока на электроде, от величины поляризации. Вид поляризационной кривой того или иного электродного процесса отражает особенности его протекания. Методом поляризационных кривых изучают кинетику и механизм окислительно-восстановительных реакций, работу гальванических элементов, явления коррозии и пассивности металлов, различные случаи электролиза. [13]
 |
Перенапряжение выделения водорода на различных металлах. [14] |
Выяснение связи между величиной поляризации и скоростью электродного процесса является важнейшим методом изучения электрохимических процессов. При этом результаты измерений обычно предоставляют в виде поляризационных кривых - кривых зависимости плотности тока на электроде от величины поляризации. Вид поляризационной кривой того или иного электродного процесса отражает особенности его протекания. Методом поляризационных кривых изучают кинетику и механизм окислительно-восстановительных реакций, работу гальванических элементов, явления коррозии и пассивности металлов, различные случаи электролиза. [15]
Страницы: 1 2