Сильная зависимость - скорость - реакция
Cтраница 1
Сильная зависимость скорости реакции от температуры облегчает установление для пламени условных пространственных границ. Фронт пламени принято разграничивать на зоны реакции и подогрева. Можно считать, что те реакции, с которыми связана основная доля тепловыделения, локализованы в зоне реакции пламени, состав которой близок к составу продуктов полного сгорания. Интенсивная реакция в этой зоне, содержащей лишь немного непрореагировавшего вещества, в основном поддерживается диффузионным переносом этих продуктов из соседней, более низкотемпературной области. В этой зоне ( подогрева) скоростью реакции можно пренебречь, однако на нее приходится большая часть перепада температуры; подогрев газа в этой зоне обеспечивается теплопроводностью из зоны реакции. [1]
 |
Разложение гексанитроэта на ( 7 пл 140 С. [2] |
Появляется сильная зависимость скорости реакции от природы и энергии решетки, которые определяют величину А -, а также от строения активированного комплекса. Увеличение энергии активации может достигать десятка килокалорий на моль. [3]
Ввиду сильной зависимости скорости реакции от температуры процессы тепловыделения и теплообмена при реакции определяют характер протекания реакции, прежде всего в процессах горения и воспламенения. Особенности режимов реакции в этих условиях рассматриваются подробно далее. [4]
Наличие в изучаемой реакции сильной зависимости скорости реакции от малых количеств ингибитора, торможение реакции при добавке ингибитора являются надежным доказательством цепного механизма процесса. [5]
При термическом распаде хлорпроизводных углеводородов наблюдается сильная зависимость скорости реакции от состояния стенок сосуда. Можно предположить, что при работе в статических условиях, в которых проведено подавляющее большинство опубликованных исследований, сходимость результатов параллельных опытов только лишь после проведения большого числа их объясняется тем, что поверхность стенок реакционного сосуда покрывается пленкой каких-то малолетучих углеродистых соединений. [6]
Для второй ( значительно более многочисленной) группы реакций наблюдается сильная зависимость скорости реакции от природы электрода. Эта зависимость связана, в первую очередь, с изменением энергии связи им-х адсорбированной частицы с поверхностью электрода. Если адсорбируется исходный реагент, то по мере увеличения энергии связи увеличивается его адсорбция ( степень покрытия поверхности), что, согласно разд. С другой стороны, то же самое увеличение энергии связи вызывает снижение энергетического эффекта qm или и - т стадии дальнейшего превращения адсорбированного реагента. [7]
Действительно, немалое влияние на развитие химии оказало убедительное подтверждение школой Оствальда [164, 167, 168] сильной зависимости скоростей реакций от пространственного строения органических молекул. [8]
Анализируемый вопрос, по-видимому, впервые был затронут Зельдовичем [1949], который отметил, что вследствие сильной зависимости скорости реакции от температуры средняя скорость реакции должна сильно отличаться от скорости реакции при средней температуре. В его работе не учтена зависимость скорости реакции от концентрации, вследствие чего сделан вывод о том, что пульсации температуры всегда приводят к увеличению средней скорости по сравнению со скоростью реакции, рассчитываемой по средним значениям температуры и концентрации. Однако, как правило, пульсации приводят к противоположному эффекту. Отметим также, что в тех точках потока, где z сильно отличается от zm, пульсации концентрации приводят к увеличению средней скорости реакций. [9]
Правда, в этой задаче за характерное времяf в течение которого происходят потери, принималось время химической реакции, которое, как уже говорилось, благодаря сильной зависимости скорости реакции от температуры очень быстро растет с уменьшением скорости детонации. Поэтому в общем виде задача решается лишь качественно и только для модели детонации Зельдовича - Неймана. [10]
При работе с жидким мономером нами было найдено, что процесс проходит с энергией активации 10 2 ккал / моль. Сильная зависимость скорости реакции от температуры нередко служит причиной неправильных выводов о влиянии отдельных компонентов на полимеризационный процесс. Поэтому кинетические измерения рекомендуется проводить в строго изотермических условиях. [11]
В момент выхода детонационного фронта из трубы в объем на его границах исчезает взаимодействие с малосжимаемой оболочкой, и в зону химической реакции начинает распространяться волна разрежения. Из-за сильной зависимости скорости реакции от давления срыв ее происходит практически сразу во фронте волны разрежения. [12]
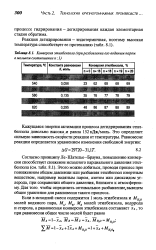 |
Конверсия этилбензола ( при разбавлении его водяным паром в мольном соотношении п. 1. [13] |
Кажущаяся энергия активации процесса дегидрирования этил-бензола довольно высока / и равна 152 кДж / моль. Это определяет сильную зависимость скорости реакции от температуры. [14]
Оптимальное соотношение компонентов катализатора связано с температурой полимеризации. Это обусловлено сильной зависимостью скорости реакции обрыва, определяющей молекулярный вес, от изменения температуры. [15]
Страницы: 1 2