Концентрационная температурная зависимость
Cтраница 2
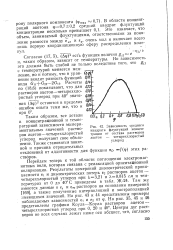 |
Зависимость среднего квадрата флуктуации концентрации от состава растворов ацетон - четыреххлористый углерод. [16] |
Таким образом, все детали в концентрационной и температурной зависимости экспериментальных значений растворов ацетон-четыреххлористый углерод получают свое объяснение. [17]
Конкретные формы полуэмпирических уравнений, описывающих концентрационную и температурную зависимость коэффициентов активности, рассматриваются в разд. Методы оценки параметров этих уравнений по экспериментальным данным о фазовых равновесиях кратко излагаются в разд. [18]
В ряде работ [34, 61-63] статическим методом были определены концентрационные и температурные зависимости коэффициентов активности летучих немезоморфных соединений в растворах и жидких кристаллах. Было установлено, что уменьшение концентрации немезогена ведет к увеличению его коэффициента активности. Если в исследуемой концентрационной области происходит фазовый переход, то это приводит к нарушению монотонного характера зависимости [34, 62], причем переход от изотропного раствора к жидкокристаллическому сопровождается резким увеличением коэффициентов активности. При неизменном агрегатном состоянии увеличение температуры приводит к уменьшению коэффициентов активности. Таким образом, выводы о влиянии температуры и агрегатного состояния на коэффициенты активности полностью совпадают с результатами, полученными методом ГЖХ. [19]
 |
Спектры поглощения гидроперекисей / г-цимола ( /, р-изопро-пилнафталина ( 2 и 1 1-дитолилэтана ( 5 в растворе СС14. [20] |
Рассматривая положение и полуширину полос поглощения, а также концентрационную и температурную зависимость спектров, можно прийти к выводу, что в молекулах гидроперекисей га-цимола, р-изопропилнафталина и 1.1 - дитолилэта а, подобно гидроперекиси кумола, имеется внутримолекулярная водородная связь гидропе-рекисной группы с я-электронами ароматической системы. [21]
 |
Концентрационная зависимость коэффициента сжимаемости у ( кроме ацсто-нитрила при 298 К в системах вода - неэлектролит. [22] |
Анализ имеющегося материала показывает, что не только качественный характер концентрационной и температурной зависимости изотермической и адиабатической сжимаемостей одинаков, но и значения Кт и Ks ( а также соответствующие парциальные величины) близки. Поэтому далее будем рассматривать их совместно, так как для многих систем имеются данные только по одному виду сжимаемости. [23]
При изучении термодинамических свойств раствора в первую очередь ставится задача определить концентрационные и температурные зависимости термодинамических функций. Допустим, найти изменение энтальпии при образовании раствора из чистых компонентов и оценить, как эта величина изменяется при изменении состава и температуры. Рассматриваются, следовательно, разности термодинамических величин для раствора и чистых компонентов; при этом по крайней мере один из компонентов - жидкость. Такая постановка задачи, диктуемая опытом, сильно облегчает теоретическое рассмотрение. Рассчитать на основании молекулярных данных полные термодинамические функции раствора - задача еще более трудная, чем в случае чистых жидкостей. Действительно, межмолекулярные взаимодействия в растворе так же интенсивны, как и в жидкости. Однако, поскольку в теории растворов ставится задача расчета разностных величин, отсчитываемых от значений термодинамических функций чистых жидкостей, проблема во многих отношениях упрощается. Более оправданным, чем в теории жидкостей, является использование моделей ( в частности, решеточных моделей): при расчете разностей ошибки в значениях термодинамических функций раствора и чистых жидкостей в какой-то степени погашаются. [24]
Пользуясь политермической характеристикой теплоемкостей той же системы, можно показать, что концентрационные и температурные зависимости этого термодинамического свойства также могут быть успешно использованы для познания природы растворов. [25]
Для определения условий проведения технологических процессов используют диаграммы состояния, которые отображают концентрационные и температурные зависимости общей свободной энергии системы и позволяют определить границы областей существования фаз, возникающих в системе. [26]
Пользуясь политермической характеристикой теплоемкостей той же системы [17], можно показать, что концентрационные и температурные зависимости этого термодинамического свойства также могут быть успешно использованы для познания природы растворов. [27]
По этой причине принят следующий порядок дальнейшего изложения. Сначала рассматриваются результаты изучения концентрационной и температурной зависимости отдельных избыточных функций: НЕ ( х), Ср ( х), GE ( x) и TSE ( x), VE ( x), при этом обсуждаются общие особенности поведения указанных функций для водных растворов неэлектролитов и делается сопоставление с аналогичными функциями для основных классов неводных растворов. В заключение дается небольшой обзор состояния статистических теорий водных растворов неэлектролитов конечных концентраций. [28]
При 150 - 300 С происходит механиче - - ское разупорядочение кристаллов КС1 и NaCl, допированных свинцом ( KCl 1 3 - 10 - 2 мол. Исследованная на тех же кристаллах концентрационная и температурная зависимость электропроводности показывает, что при этих температурах крупные примесные центры разбиваются на диполи ион - примеси - катионная вакансия. [29]
На их основе удалось вскрыть многие закономерности концентрационной и температурной зависимости термодинамических функций, хотя очевидно, что предположение о расположении молекул в узлах правильной решетки, не отражает действительную структуру жидких систем. [30]
Страницы: 1 2 3