Термодинамическая зависимость
Cтраница 1
Термодинамические зависимости для перхлорилфторида28 рассчитаны при 100 - 5000 К. [1]
Термодинамическая зависимость между потенциалами электрода и константой равновесия обратимой химической реакции на электроде позволяет приближенно рассчитать изменения концентрации потенциалопределяющего иона ( ОН -), если принять, что электрохимическая цепь находится в состоянии, при котором концентрация ионов ОН равна единице. [2]
Термодинамические зависимости имеют основное значение в выборе надлежащих условий проведения препаративных реакций. В тех случаях, когда необходимые данные отсутствовали, была сделана попытка оценить термодинамические функции настолько точно, насколько это возможно. [3]
 |
Отсчеты на диаграмме s - Т.| Отсчеты на диаграмме Т - 1.| Огсче - /. ты на диаграмме / - Igp. [4] |
Все термодинамические зависимости реального газа достаточно точно графически отображаются на этих диаграммах. Протекающие в холодильных аппаратах процессы наглядно иллюстрируются диаграммами, по которым легко производить необходимые отсчеты. [5]
Формулы термодинамических зависимостей, выведенные для идеальных растворов ( главы III и IV), можно применять к реальным растворам лишь при условии, что эти растворы бесконечно разбавлены. [6]
При известной термодинамической зависимости е ( р, р) уравнение (5.29) дает связь между значениями давления и плотности за разрывом. Поток F входит в него в качестве параметра. [7]
В термодинамических зависимостях часто пользуются физической величиной, называемой теплоемкостью. [8]
Напомним некоторые термодинамические зависимости, известные из физической химии. Для подавляющего большинства химических процессов, идущих при постоянном давлении, мерой их самопроизвольности является изобарно-изотермический потенциал ( энергия Гиббса) AG, равный разности этих потенциалов для продуктов и реагентов. [9]
Графическое изображение термодинамических зависимостей в виде диаграмм состояния позволяет наглядно представить все основные термодинамические процессы и достаточно точно произвести необходимые отсчеты. [10]
Графическое изображение термодинамических зависимостей в виде диаграмм состояния позволяет наглядно представить все основные термодинамические процессы и достаточно точно произвести необходимые отсчеты. Ими чаще всего пользуются при расчетах холодильных процессов. [11]
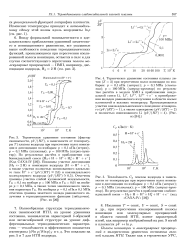
Волнообразная структура термодинамических зависимостей НТП, на уровне уравнения состояния, эквивалентна характерной ( - образной или зигзагообразной структуре на уровне дифференциальных термодинамических характеристик - теплоемкости и эффективного показателя изоэнтропы ( д пр / д пр и Т - Д - Это показано на рис. 5 и 7 для НТП водорода. [13]
Это сильно упрощает термодинамические зависимости. [14]
В силу природы термодинамических зависимостей сходимость решения не может быть достигнута при первой итерации, поэтому первый расчет паровой фазы по идеальным законам не приведет к значительным ошибкам. [15]
Страницы: 1 2 3 4