Линейная зависимость - скорость - реакция
Cтраница 1
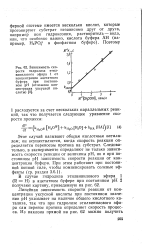 |
Зависимость скорости гидролиза этил-винилового эфира 1 от концентрации ацетатного буфера при постоянном рН ( отложена концентрация уксусной кислоты. [1] |
Линейная зависимость скорости реакции от концентрации уксусной кислоты при постоянном значении рН указывает на наличие общего кислотного катализа, так что при гидролизе этилвинилового эфира сам перенос протона определяет скорость процесса. [2]
Линейная зависимость скорости реакции от концентрации мономера, отмеченная некоторыми авторами, справедлива лишь в грубом приближении. С ростом концентрации триэтилалюминия падает молекулярный вес и повышается содержание изотактического полимера. Эти изменения, впрочем, не настолько существенны, чтобы представлять технический интерес. В зависимости от концентрации мономера несколько возрастают молекулярный вес и содержание фракций, экстрагируемых н-гептаном. [3]
На рис. 1 и 2 показана линейная зависимость скорости реакции от давления кумола. [4]
К сожалению, невозможно сказать, даст ли график линейной зависимости скоростей реакций в стационарном состоянии ( либо по Лайнуиверу-Бэрку, либо по Идаю) значение К или / См. Интересно вычислить / См при различных температурах и таким образом установить соотношение между стабильностью комплекса, его реакционной способностью, выраженными соответственно через / См и k3, с одной стороны, и его химическим составом и строением - с другой. Как ни парадоксально, эти сведения можно получить для некоторых бимолекулярных реакций на основании метода стационарных состояний ( в действительности определить ki и kz, а также ks), несмотря на то что кинетика этих реакций сложнее, чем рассмотренная здесь; это оказывается возможным потому, что второй субстрат допускает изменение еще одного фактора, влияющего на скорость, и, следовательно, дает возможность вывести иное уравнение, связывающее константы другим способом. В некоторых реакциях каталазы и пероксидазы удавалось проследить [20] за ростом концентрации комплекса фермент - субстрат на ранних стадиях реакции при использовании методики быстрого смешивания и при спектрофотометрическом измерении концентрации комплекса. [5]
Основным параметром, определяющим скорость реакции, является давление водорода: наблюдается линейная зависимость скорости реакции от парциального давления водорода; давление же окиси углерода должно лишь обеспечить стабильность каталитического комплекса в растворе. [6]
При протолизе метилмеркуриодида уксусной кислотой в ацетатном буфере при 161 С также обнаружена линейная зависимость скорости реакции от концентрации кислоты. В связи с этим сделано заключение о существовании общего кислотного катализа. Таким образом, в переходном состоянии связь О - Н кислоты лишь слегка ослаблена, а связь С - Н только начинает зарождаться. [7]
Интерпретация кинетических данных типа: отсутствие зависимости скорости реакции от концентрации буфера означает специфический катализ или линейная зависимость скорости реакции от концентрации буфера означает общий катализ - не является обязательной, поскольку существует несколько возможных механизмов, которые дают одну и ту же кинетическую картину. [8]
Полученное соотношение показывает, что линейная зависимость стехиометрических уравнений реакций не влечет за собой в общем случае линейной зависимости скоростей реакций. [9]
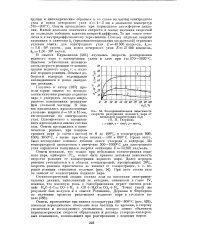 |
Экспериментальная зависимость. [10] |
Опыты показали, что только при небольших концентрациях водяного пара, примерно 5 /, может быть принята линейная зависимость скорости реакции от концентрации водяного пара. При этом состав газа не зависит от концентрации водяного пара. [11]
Однако в границах указанных выше концентраций, несмотря на значительные изменения в степени агрегации ( особенно в бензоле), линейная зависимость скорости реакции от концентрации катализатора сохраняется. [12]
Лаба - тон127 нашел, что скорость фторирования трехфтористым хлором в азоте возрастает до максимума при 105 С, затем падает до некоторого минимума при 148 С и далее снова возрастает. Как и в случае фтора, была найдена линейная зависимость скорости реакции от парциального давления C1F3 при 17 С. [13]
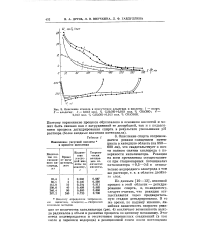 |
Окисление этанола в присутствии альдегида и кислоты. 1 - спирт. 2 - альдегид. 3 - 0 013 мол. % С2Н5ОН 0 013 мол. % СН3СНО. 4 - 0 013 мол. % С2Н5ОН 0 013 мол. % СН3СООН. [14] |
По данным [10-13], основной процесс в этой области - дегидрирование спирта, и, по-видимому, следует считать, что реакция осуществляется через предварительную стадию дегидрирования. В то же время, по нашему мнению, линейная зависимость скорости реакции от количества катализатора ( рис. 4) исключает возможность выхода радикалов в объем и развитие процесса по цепному механизму. [15]
Страницы: 1 2