Очень сильное основание
Cтраница 1
Очень сильные основания характеризуются тем, что связдн-ная с ними кислота имеет чрезвычайно слабую диссоциацию. [1]
Это очень сильное основание, оно действует как катализатор потому, что ОН-группа образует гораздо более эффективную мостиковую связь, чем ОН2 - группа. [2]
Применение очень сильного основания и апротонного растворителя позволяет избирательно провести перекрестную альдольную конденсацию даже с участием несимметричного кетона. [3]
С очень сильными основаниями происходит первичное отщепление протона, аналогичное flcb - механизму, и промежуточно образуется дегидробензол. Такой механизм доказывается с помощью меченых атомов. [4]
При действии очень сильных оснований алкины, имеющие концевую тройную связь, полностью ионизируются и образуют соли, которые называют ацетиленидами. Например, при пропускании над металлическим натрием, нагретым до 150 С, ацетилен превращается в натрийацетиленид. [5]
В присутствии очень сильных оснований енолизируемый эфир, например этилпропаноат, практически нацело подвергается ионизации. [6]
При действии очень сильных оснований типа бутиллитил гидри / а натрия на JS-кетоэфиры удается осуществить алкилирование иди апилирование этих соединений по менее кислому у-углеродному атому. [7]
Последняя представляет собой очень сильное основание, близкое по свойствам к щелочам; при взаимодействии с кислотами образует с выделением воды соли тетраметиламмония. [8]
Последняя представляет собой очень сильное основание, близкое по свойствам к щелочам; при взаимодействии с кислотами образует с выделением воды соли тстраметиламмоння. [9]
Только в случае очень сильного основания получаются соединения со свойствами динамических структур. [10]
Однако при действии очень сильных оснований амины образуют соли, причем анионы в этих солях, в свою очередь, также являются сильными основаниями. [11]
 |
Кислотность СИ связен в ДМСО и газовой фазе ( подчеркнуты наиболее кислые протоны. [12] |
Большинство карбаннонов являются очень сильными основаниями, и поэтому их нельзя получить в высокой концентрации из соответствующих СН-кислот в водных или спиртовых растворах щелочей. Данные по кислотности СН-кислот в ДМСО приведены в табл. 3.15, в которую для сравнения включены также некоторые ОН -, NH - и другие типы кислот, а также величины сродства к протону карбаннонов в газовой фазе ( см. разд. Для карбаннонов, рКа которых больше, чем рКа ( ДМСО) 35 1, истинные значения могут сильно отличаться от приведенных в таблице ориентировочных значений. Для таких карбаннонов величины рКа оцениваются по кинетической СН-кислотности, т.е. по скоростям отрыва протона от СН-кислот, которые связаны с величинами рКл соотношением Бренстеда. [13]
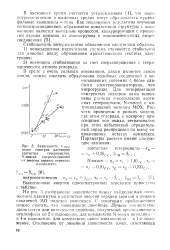 |
Зависимость v макс полос спектров растворов азотистых гетероциклов, N-окисей. нитросоединетш от энергии первого перехода сг-комплекса. [14] |
В среде с очень сильным основанием, каким является анион амида, можно ожидать образования подобных соединений в ненасыщенных системах с более слабыми электроноакцепторами, чем нитрогруппы. Для интерпретации измеренных спектров нами выполнены расчеты сг-комплексов азотистых гетероцпклов, N-окисей и ни-тросоединений методом МОХ. Расчеты проведены в рамках модели, где атом углерода, к которому присоединен нон амида, тетрагонален; при этом избыточный отрицательный заряд распределен по всему сопряженному остатку комплекса. [15]
Страницы: 1 2 3 4