Основность - катализатор
Cтраница 1
Основность катализатора не коррелирует с энергиями активация, вероятно, вследствие сильного конкурирующего действия катиона. У Li2S04 и других сульфатов щелочных металлов мы обнаружили, однако, настолько низкую каталитическую активность, что ее трудно было оценить. Это можно объяснить только тем, что катион оказывает стабилизирующее действие на образующийся карбанион; следовательно, одновалентные катионы обладают слишком слабым стабилизирующим действием. [1]
Основность катализатора, согласно проведенному обзору, существенно увеличивает скорость реакций изомеризации олефинов с перемещением двойной связи, конденсации многих органических соединений с отщеплением воды, некоторых реакций полимеризации. Увеличение избыточного заряда на этих ионах приводит к способности твердых оснований в некоторых случаях катализировать гомолитические реакции, например, дегидрирование спиртов и углеводородов. [2]
Скорость реакции увеличивается с увеличением основности катализатора и уменьшением температуры, что авторы связывают с механизмом обрыва, имеющим высокую энергию активации. [3]
 |
Метиленовые компоненты и катализаторы, используемые в реакциях конденсации. [4] |
СН-Кислотность метиленовых компонентов уменьшается, а основность катализаторов увеличивается в направлении сверху вниз. [5]
Равновесие в первой стадии реакции зависит от основности катализатора и от кислотности атома водорода, находящегося в - положении сложного эфира. Третья стадия происходит быстро, однако равновесие благоприятствует образованию ацетоацетат-аниона, поскольку он - наиболее слабое из всех присутствующих оснований и поэтому наиболее стабильный. Если ( З - кетоэфир не может образовать анион, как, например, этиловый эфир изобутир ил изомасляно и кислоты, вместо этилата натрия следует применять сильный основной катализатор трифеншшетилнат-рий. В этом случае этилат-ион, продукт конденсации, будет более слабым основанием, чем ион трифенилметила, что тем самым благоприятствует образованию этилата, трифенилметана и 5-кетоэфира. Конденсация смешанных эфиров, обычно происходящая при взаимодействии большого избытка этилового эфира щавелевой кислоты, этилового эфира трифтор уксусной кислоты, метилового эфира пиколиновой кислоты, этилового эфира бензойной кислоты или этилового эфира изомасляно и кислоты и некоторых других эфиров с соединениями, содержащими активную метиленовую группу, например этиловым эфиром пропионовой кислоты, за последнее время улучшена за счет применения основного катализатора, диизопро-пиламиномагнийбромида. Очевидно, катализатор способствует превращению сложного эфира, имеющего активную метиленовую группу, нацело в анион. [6]
Величины аир показывают чувствительность данной реакций к изменениям кислотности или основности катализатора, причем аир всегда меньше единицы, но больше нуля. В логарифмических координатах ( рис. 27) уравнение соответствует прямой, по тангенсу угла наклона которой находят а ( или р), а по отрезку на оси ординат - IgG. & и / Сь часто неизвестны, и в этом случае используют значения, найденные для водных растворов. Это позволяет применять уравнение Бренстеда лишь для структурно подобных кислот и оснований. [8]
Полимеризация других карбонильных мономеров происходит подобным же образом, однако основность требующегося катализатора может быть существенно различной. [9]
Анионная полимеризация в присутствии оснований должна происходить тем легче, чем выше основность катализатора и выше сила мономера как кислоты Льюиса. Результаты представлены в таблице. В первой графе указаны вещества, применяемые в форме натриевого соединения в качестве оснований. [10]
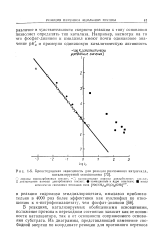 |
Бренстедовская зависимость для реакции разложения нитрамида, катализируемой основаниями. [11] |
В реакциях, катализируемых обобщенными основаниями, положение протона в переходном состоянии зависит как от основности катализатора, так и от основности сопряженного основания субстрата. [12]
Бар-Эли и Клейн [8] распространили эту реакцию на амины и показали, что скорость изотопного обмена водорода с молекулярным дейтерием растет с увеличением основности катализатора. [13]
Основность катализатора, требующаяся для инициирования полимеризации, зависит от характера заместителей у карбонильной группы. [14]
В результате получается макромолекула с регулярным чередованием звеньев. Чем больше основность катализатора, тем активнее он катализирует анионную полимеризацию. Обрыв цепи при анионной полимеризации происходит обычно путем ее передачи на растворитель или мономер. [15]
Страницы: 1 2
