Особенность - равновесие
Cтраница 1
Особенность равновесия при удалении ионов металлов выражается в том, что не наблюдается никакой разницы при параллельном сравнении его с равновесным состоянием одно-полярных катионо - и соответственно анионо-обменных смол. [1]
На этой особенности равновесия данной химической реакции основан металлургический процесс цементационного выделения меди из цинксодержащих растворов. [2]
Теперь рассмотрим особенности равновесия между фазами в том случае, когда из раствора ( или расплава) кристаллизуется в виде твердой фазы только один из компонентов ( условно будем в дальнейшем называть его растворителем), а второй компонент присутствует только в растворе. [3]
Рассмотренные выше простейшие примеры не исчерпывают всех особенностей равновесий с растворителем. Возможность образования комплексных ионов, состав которых изменяется с рН, гидроксидов и основных солей значительно усложняет взаимодействия с растворителем. [4]
 |
Результаты расчета процесса укрепления водных растворов формальдегида ректификацией при пониженном давлении. [5] |
Характерная черта ректификации водных растворов формальдегида, связанная с особенностями равновесия между жидкостью и паром - близость температур верха и куба. [6]
Квазистационарной эта последовательность становится лишь тогда, когда в силу особенностей равновесия промежуточной стадии 2 скорости медленных стадий 1 и 3 несоизмеримы, так что наиболее медленная ( лимитирующая) стадия оказывается единственной. [7]
При измерениях влажности необходимо учитывать формы ее связи с материалом, а также особенности гигротермического равновесия материала с окружающей воздушной средой. [8]
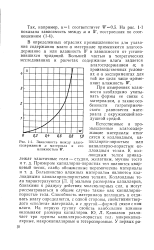 |
Зависимость между влагосодержанием и материала и его влажностью W. [9] |
При измерениях влажности необходимо учитывать формы ее связи с материалом, а также особенности гигротермиче-ского равновесия материала с окружающей воздушной средой. [10]
 |
Реакционные узлы для дегидрирования этилбензола. [11] |
На новых установках применяют поэтому иные конструкции реакционного узла, приближающие процесс к изотермическому и лучше учитывающие особенности равновесия реакции. В одном из них ( рис. 138 6) имеются два реактора ( или два слоя катализатора); охладившуюся в первом аппарате смесь до подачи во второй подогревают перегретым паром до 600 - 630 С. Реактор, изображенный на рис. 138, в, имеет два-три кольцевых слоя катализатора, причем в первый слой поступает весь этил-бензол, но лишь часть водяного пара. В пространство между слоями катализатора подают дополнительное количество перегретого пара; с его помощью повышается температура смеси, происходит ступенчатое разбавление смеси, что приводит к отклонению ее параметров от равновесного состояния и способствует росту скорости и селективности реакции. В этих новых установках при сохранении высокой селективности ( 89 - 90 %) достигаются большие степени конверсии ( 60 - 75 %) и интенсивность процесса ( объемная скорость 0 5 - 0 6 ч -), снижается удельный расход пара. [12]
 |
Реакционные узлы для дегидрирования этилбензола ( ЭБ. [13] |
На новых установках применяют поэтому иные конструкции реакци энного узла, приближающие процесс к изотермическому и лучше учитывающие особенности равновесия реакции. [14]
Мы уже познакомились с представлением о равновесии между двумя или тремя состояниями системы, но необходимо остановиться еще на одной особенности равновесий. [15]
Страницы: 1 2