Падение - энергия
Cтраница 1
Падение энергии при увеличении времени связано с тем, что: при распространении не бесконечно слабой звуковой волны часть энергии необратимо переходит в тепловую энергию, которая застревает сзади волны, прошедшей через данный объем воздуха. Можно учесть и этот эффект: мы знаем, что при определении Я0, MO и / 0 неточность, связанная с пренебрежением изменения энтропии, не сказывается на членах 2-го порядка малости, пропорциональных ( Др) 2 - ч, которые после интегрирования становятся членами 1-го порядка малости. [1]
Поэтому падение энергии связи водорода с поверхностью металла при уменьшении числа неспа-репных электронов в of - зонс в ряду железо, кобальт, никель приводит к увеличению удельной каталитической активности. При переходе к следующему металлу - меди, с заполненной rf - зоной, энергия связи водорода с поверхностью металла и скорость хемосо-рбции резко уменьшаются. В соответствии с этим очень мала и удельная каталитическая активность меди в отношении реакции обмена атомами водорода. [2]
 |
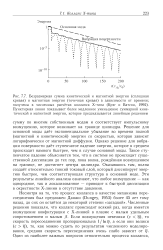
Фрагмент развертки поля излучения лазера с бифокальной термической линзой. свободная генерация, активный элемент из стекла ГЛС-2 ( 07 X 130 мм, L 38 см, Р 750 Вт. [3] |
Зависимость степени падения энергии ( роста потерь) от величины Q ( см. рис. 2.30) также находит качественное объяснение в этой модели. [4]
Накопление гидроксильных групп у концевых углеродных атомов углеводородных цепей обусловливает падение энергии адсорбции прежде всего за счет увеличения растворимости этих соединений. Естественно, что при длине углеводородного радикала органического компонента, соизмеримой с полостями клатратных структур воды, влияние гидроксильной группы на растворимость вещества оказывается небольшим. [5]
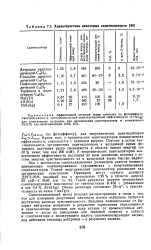 |
Характеристики некоторых сцинтилляторов. [6] |
Кроме того, у органических сцинтилляторов конверсионная эффективность уменьшается с падением энергии. У неорганических сцинтилляторов конверсионная эффективность постоянна во всем диапазоне, поэтому с ростом энергии чувствительность их к воздушной керме быстро падает. [7]
 |
Общий вид ускорителя ИЛУ-2 для ионного легирования полупроводников. Создан в Институте атомной энергии имени И. В. Курчатова. [8] |
Это обусловлено сложным взаимодействием, возникающим между примесными атомами и падением энергии их ионизации до нуля. Если концентрация примеси достигает 1019 в 1 см3, полупроводник перестает быть полупроводником: он начинает проявлять свойства металла с высоким электросопротивлением. [9]
 |
Зависимость удельной энергии на единицу веса разных типов аккумуляторов от развиваемой ими удельной мощности. [10] |
При больших мощностях разряда это соотношение увеличивается, так как у свинцовых и кадмиево-никелевых аккумуляторов падение энергии с ростом мощности выражено более резко, чем у серебряно-цинковых. [11]
На основании многочисленных опубликованных в литературе экспериментальных данных по поводу чувствительности к надрезу стали и общеизвестного факта падения энергии при ударе, в так называемом ударном испытании надрезанного образца при температурах около ( и ниже) 0 С, можно ожидать, что при низких температурах наличие в резервуарах или корабельных плитах небольших дефектов может привести к катастрофическому разрушению, даже если ударных нагрузок и нет. Поэтому можно с уверенностью утверждать, что опасное образование трещин отрыва вызвано следующими факторами. [12]
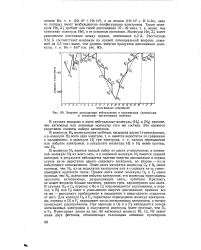 |
Энергия диссоциации нейтральных и заряженных ( катионных и анионных двухатомных молекул. [13] |
В молекуле N2 имеется полный набор из шести р-электронов; в катион-ной молекуле NJ их всего пять, а в анионной молекуле Ni имеется лишний электрон; в результате наблюдается падение энергии диссоциации в первом случае из-за недостатка одного связевого электрона, во втором - из-за избыточного антисвязевого. Левее азота находятся молекулы G2 и В2 менее прочные, чем N. Правее азота лежат молекулы О2 и F2 менее прочные, чем N2, вследствие избытка электронов: эти молекулы принуждены заполнять антисвязевые, разрыхляющие связь, орбитали. Кратность не может возрасти больше значения, равного трем, характерного для азота. В случаях В2 и С2 переход к Bi и Q сопровождается упрочнением, а переход к BJ или С ведет к уменьшению энергии диссоциации: причина все та же - выгодность приближения к насыщению и невыгодность отдаления от него. Для молекул О2 и Ра характерно пересыщение молекул электронами; переход к Oi и F наращивает число антисвязевых электронов, а потому происходит разупрочнение. [14]
Страницы: 1 2 3