3-нитропиридин
Cтраница 1
Восстановление 3-нитропиридина и щелочное плавление 3-пири-динсульфокислоты приводит соответственно к 3-аминопиридину и 3-оксипиридину. [1]
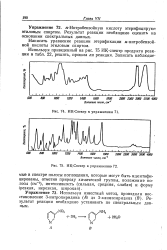 |
ИК-Спектр к упражнению 72. [2] |
Используя известный метод, проводили восстановление 3-нитропиридина ( А) до 3-аминопиридина ( В), Результат реакции необходимо установить по спектральным данным. [3]
Прямое нитрование пиридина требует жестких условий н приводит к 3-нитропиридину с небольшим выходом. Фридль 11 ], впервые успешно осуществивший эту реакцию, при нитровании пиридина нитратом калия в растворе серной кислоты, нагретой до 300, получил 3-нитропиридин с 15-процентным выходом. [4]
Восстановлением в аминопиридин, который был идентифицирован как [ З - аминопиридин, Фридль доказал, что продукт нитрования является ( 3-нитропиридином. В данном случае подтвердилось правило, что присутствие третичного атома азота ориентирует заместители отрицательного характера, прежде всего, в ( 3-положение. [5]
Анион-радикал 2-хлор - З - нитропиридина разлагается в течение 1 ч, восстановление нейтральной молекулы при более отрицательных потенциалах приводит к анион-радикалу 3-нитропиридина, Остальные из перечисленных нитропиридинов дают устойчивые продукты одноэлектронного восстановления. [6]
Сам пиридин ( рДа 5 23) в виде пиридиниевого катиона нитруется с большим / трудом, давая даже при нагревании c KNO в олеуме до 300 С 3-нитропиридин с очень низким выходом. Введение электронодонорных заместителей облегчает нитрование пиридиниевых ионов. [7]
Каковы структурные формулы следующих соединений: 1) а-аминопиридина, 2) 2-оксипиридина ( тау-томерные формы), 3) 4-оксипиридина ( таутомерные формы), 4) 3-нитропиридина, 5) гидроксида 4-метилпи-ридиния, 6) иодида М - метилпиридиния, 7) у-метилпири-дина, 8) 2-метил - 5-винилпиридина, 9) 2-метилхинолина. [8]
При этом получается 3-нитропиридин с выходом, составляющим всего несколько процентов. При нитровании 2-метилпиридина в аналогичных условиях получается 2-метил - 5-нитро-пиридин тоже с небольшим выходом. [9]
Иначе ведут себя шестичленные гетероциклические соединения. Пиридин переводится в ( 3-нитропиридин с исключительным трудом и с очень плохими выходами. Эта малая склонность к нитрованию распространяется и на хинолин, в котором нитруется только бензольная половина. Пиразол снова гладко нитруется как обычное ароматическое соединение. Невидимому, реакционная способность системы объясняется наличием групп NH. Изоксазолы, замещенные в положениях 3 5, тоже гладко переходят в нитропроизводные. [10]
Большинство этих р-ций протекает в кислой среде, в к-рой исходным соед. С, образуя с небольшим выходом 3-нитропиридин; сульфируется олеумом в присут. [11]
Реакции электрофильного замещения в соответствии с выше отмеченными представлениями о строении пиридина протекают избирательно в р-положении, в условиях более жестких, чем для бензола. Так, пиридин сульфируется олеумом при 230СС в присутствии солей двухвалентной ртути, нитруется с незначительным выходом в 3-нитропиридин и хлорируется в газовой фазе при высокой температуре. [12]
Реакции электрофильного замещения в соответствии с выше отмеченными представлениями о строении пиридина протекают избирательно в р-положение, в условиях более жестких, чем для бензола. Так, пиридин сульфируется олеумом при 230 С в присутствии солей двухвалентной ртути; нитруется с незначительным выходом в 3-нитропиридин и хлорируется в газовой фазе при высокой температуре. [13]
Нитрование пиридина также требует более жестких условий. Действие раствора нитрата калия в азотной кислоте на раствор пиридина в 100 % - ной серной кислоте при 300 в присутствии железного катализатора дает 3-нитропиридин с 22 % - ным выходом. [14]
Нитрование пиридина также требует жестких условий. Действие раствора нитрата калия в азотной кислоте на раствор пиридина в 100 % - ной серной кислоте при 300 С в присутствии железного катализатора дает 3-нитропиридин с 22 % - ным выходом. [15]
Страницы: 1 2