Пектолит
Cтраница 1
Пектолит отличается от волластонита по положительному удлинению и большему двупреломлению. [1]
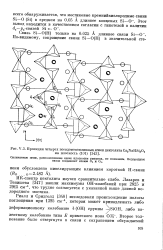 |
Проекция четырех псевдомоноклинных ячеек пектолита Ca2NaHSi309 на плоскость ( 101. [2] |
ИК-спектр пектолита изучен сравнительно слабо. Лазарев и Тенишева [347 ] нашли максимумы ОН-колебаний при 2825 и 2915 см 1, что трудно согласуется с указанной выше длиной водородного мостика. [3]
Для получения пектолита Ca2NaHSi3O9 Тило, Функ и Вих-ман [309] рекомендуют произвести осаждение аморфной фазы из раствора Na2H2Si04 - 8H20 с помощью насыщенного раствора Са ( ОН) 2, взятого в избытке. [4]
Белянкина и Ивановой82 касается распада пектолита при прокаливании выше 700 С. После непрерывной дегидратации пектолит распадается на р-метасиликат кальция и стекло. Эти авторы предполагают возможность небольшой примеси метасиликата натрия в структурах а - и р-метасиликатов кальция. [5]
Как было показано на рис. 5.1, в состав цепочечных силикатов входит группа минералов - пироксеноидов, представляющая следующие минералы: бустамит, волластонит, пектолит, пироксмантит, родонит и серандит. Данный минерал встречается в виде белых, сероватых, желтоватых, красноватых или коричневато-белых массивных, волокнистых или плотных агрегатов. [6]
Белянкина и Ивановой82 касается распада пектолита при прокаливании выше 700 С. После непрерывной дегидратации пектолит распадается на р-метасиликат кальция и стекло. Эти авторы предполагают возможность небольшой примеси метасиликата натрия в структурах а - и р-метасиликатов кальция. [7]
Разложению предшествует постепенное выделение воды, связанной с дефектными местами структуры, или адсорбированной мелкими кристалликами. При нагревании в токе сухого воздуха пектолит теряет воду в более широком температурном интервале, начиная с 400 С. Аналогичным образом ведет себя синтетический пектолит. [8]
В кристаллах с бесконечными цепными анионами встречаются сильные водородные связи внутриионного типа. Надежно установлено наличие таких связей в структуре пектолита Ca2Na ( HSi309) [ 1, стр. [9]
ОН), выполнив свои функции, либо возвращаются в исходный раствор, либо перескакивают в окружение катиона Са ( Са-хлорортосиликат); они также могут оставаться и у своих прежних хозяев - в координационной сфере кремния. Это подтверждается наличием в структурах ГСК ( афвиллит, булфонтейнит, пектолит, розенханит) [ 5Ю3бН ] - тетраэдров. [10]
Разложению предшествует постепенное выделение воды, связанной с дефектными местами структуры, или адсорбированной мелкими кристалликами. При нагревании в токе сухого воздуха пектолит теряет воду в более широком температурном интервале, начиная с 400 С. Аналогичным образом ведет себя синтетический пектолит. [11]
Поскольку сильные основания со слабыми и сильными кислотами дают кислые соли, а слабые основания - - основные ( в особенности со слабыми кислотами), то силикаты, как соединения в подавляющем числе случаев слабых оснований ( Fe, Al, Si), по-видимому, никогда не являются кислыми солями. Сильные основания ( Са, К, Ва), часто находящиеся в силикатах, вряд ли перекрывают действие слабых оснований, обычно присутствующих в большем количестве. Исключением могут явиться, пожалуй, только минералы группы пектолита HNaCa jSisOg ], исследование структуры которых представляло бы с этой точки зрения большой интерес. [12]
Поскольку сильные основания со слабыми и сильными кислотами дают кислые соли, а слабые основания - основные ( в особенности со слабыми кислотами), то силикаты, как соединения в подавляющем числе случаев слабых оснований ( Fe, A1, Si), по-видимому, никогда не являются кислыми солями. Сильные основания ( Са, К, Ва), часто находящиеся в силикатах, вряд ли перекрывают НО. Исключением могут явиться только минералы группы пектолита ] ШаСа2 [ 81з09 ], исследование структуры которых представляло бы с этой точки зрения большой интерес. [13]
Страницы: 1